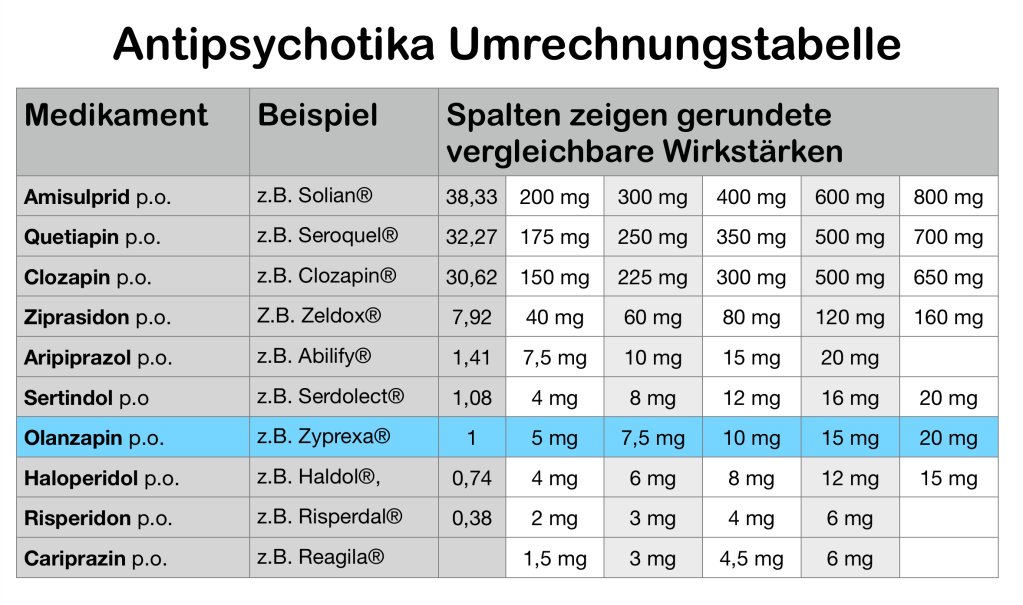
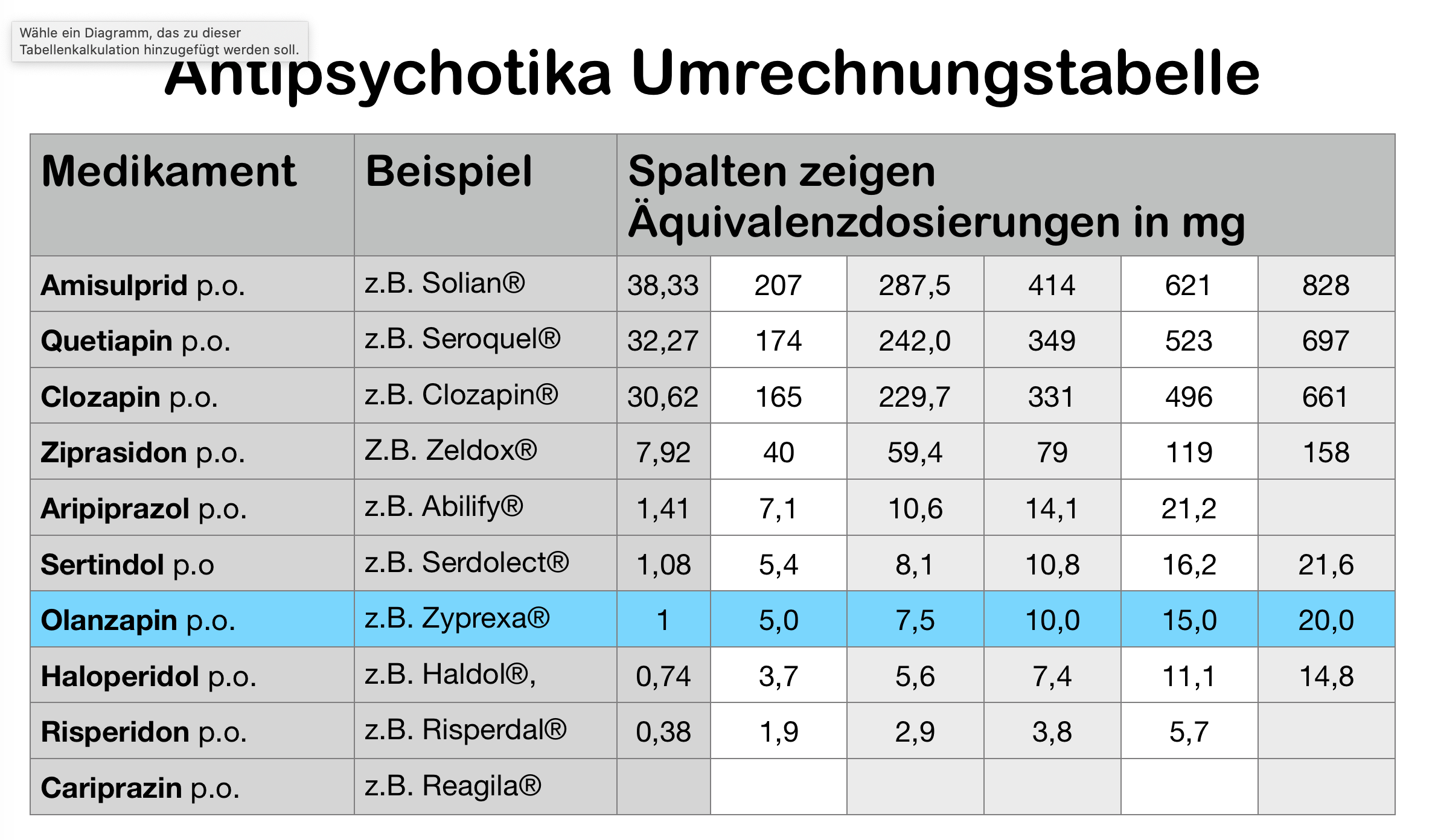
Ich habe das Kapitel für die nächste Auflage meines Buches (die aber nicht vor 2023 kommen wird) überarbeitet, besser lesbar gemacht und übersichtlicher gestaltet. Wie es gute alte Tradition ist, veröffentliche ich hier den Textentwurf (dieser Text steht daher ausnahmsweise unter Copyright). Ich bitte euch, mir Rückmeldung zum Text zu geben, auf Fehler oder Unvollständigkeiten hinzuweisen und mir zu sagen, wie ich es verständlicher beschreiben könnte.
Ich habe dieses Kapitel auch als Video eingesprochen, das findest Du hier.
Ansonsten: viel Spaß mit diesem Kapitel zu Risperidon!
5.3.1 Risperidon
Risperidon
- ist ein atypisches Antipsychotikum
- ist meist stark und sicher wirksam
- ist in Dosierungen bis 3 mg pro Tag meist gut verträglich
- kann, insbesondere bei höheren Dosierungen als 4 mg/Tag, EPMS auslösen.
- verursacht selten relevante Müdigkeit, Gewichtszunahme, QTc-Zeit-Verlängerung oder ein metabolisches Syndrom
- ist für viele Psychiater das Antipsychotikum der 1. Wahl.
Risperidon ist ein lange etabliertes atypisches Antipsychotikum, das viele Psychiater als Mittel der ersten Wahl bei psychotischer Symptomatik einsetzen. Es wirkt über einen Dopamin-D2-Antagonismus sowie zusätzlich über einen 5-HT2-Antagonismus. Daraus leitet sich seine meist sichere antipsychotischer Wirkung und oft gute Verträglichkeit ab.
Es steht als eines von nur 17 Psychopharmaka verdientermaßen auf der Liste der unentbehrlichen Arzneimittel der WHO.
Pharmakologie
Risperidon (siehe Abb. 4.4) blockiert zum einen wie ein typisches Neuroleptikum den Dopamin-D2 -Rezeptor, und zum anderen wie viele atypische Neuroleptika den Serotonin-5HT2A -Rezeptor. Es verursacht nur in geringem Maße Gewichtszunahme und Müdigkeit, entsprechend seiner nur geringen, aber vorhandenen Aktivität am Histamin H1 -Rezeptor.

Risperidon selbst hat eine Halbwertszeit von 2-4 Stunden, sein aktiver Metabolit 9-Hydroxy-Risperidon eine von ca. 20 Stunden.
Die Metabolisierung erfolgt hauptsächlich in der Leber über CYP2D6 zum aktiven Metaboliten Paliperidon.
Wenn man den Blutspiegel bestimmt, orientiert man sich nicht am Wert für Risperidon alleine, sondern an der Summe aus Risperidon und 9-Hydroxy-Risperidon. Diese sollte zwischen 20 und 60 ng/ml liegen. Ab 40 ng/ml können gehäuft Nebenwirkungen auftreten.
Klinischer Einsatz
Risperidon ist schnell und zuverlässig wirksam. Die häufigste Indikation ist die Behandlung schizophrener Psychosen. Darüber hinaus wird es in niedrigeren Dosierungen auch bei Manien, Depressionen mit psychotischer Symptomatik und aggressivem Verhalten eingesetzt.
Schizophrenie
Aufgrund seiner guten Verträglichkeit und seiner sicheren Wirkung wird es von vielen Psychiatern als Medikament der 1. Wahl bei schizophrenen Psychosen eingesetzt.
Akute psychotische Episoden bei sonst gesunden Erwachsenen kann man gut mit 3-4 mg Risperidon behandeln. Darunter klingen die Halluzinationen oft nach ca. 10 Tagen ab, der Wahn verbessert sich oft innerhalb der ersten 3-4 Wochen. Wenn die Dosis nicht ausreicht, kann man auf bis zu 6 mg/ Tag steigern, allerdings treten hier häufiger Nebenwirkungen auf, insbesondere EPMS.
Wenn Risperidon in der Akutphase gut gewirkt hat, kann man es gut in etwas niedrigerer Dosis als Rezidivprophylaktikum weiter geben. Hier sind die erforderlichen Dosierungen schwerer anzugeben, manche älteren Patienten kommen mit 0,5-1 mg gut hin, viele erwachsene Patienten erhalten 1,5 bis 3 mg als Rezidivprophylaxe, einige chronisch Kranke brauchen auch 6 mg zur Erhaltungstherapie. Die Wirksamkeit der gewählten Dosis kann man erst einem oder besser zwei Jahren beurteilen, wenn man weiß, ob ein Wiederauftreten der Krankheit verhindert worden ist.
Für die Rezidivprophylaxe ist eine gute Verträglichkeit unabdingbar, sonst wird das Medikament erfahrungsgemäß schnell abgesetzt. Risperidon bietet in vielen Fällen auch bei niedrigeren und gut verträglichen Dosierungen einen guten Rückfallschutz.
Einige Patienten bevorzugen die Rezidivprophylaxe mit einem Depot-Antipsychotikum, hier stehen Risperidon und sein gleichstark wirksamer Metabolit Paliperidon für unterschiedliche Dosierungsintervalle zur Verfügung:
- RisperdalConsta® (Risperidon, alle zwei Wochen)
- Xeplion® (Paliperidon, alle vier Wochen)
- TREVICTA® (Paliperidon, alle 12 Wochen)
Manie
Akute Manien sollten immer mit einer Kombination aus einem Phasenprophylaktikum, vorzugsweise Lithium, und einem Antipsychotikum behandelt werden. In dieser Indikation wird Risperidon oft zwischen 2 und 4 mg/Tag dosiert, in der Gerontopsychiatrie zwischen 0,5 und 2 mg/Tag.
Nach Abklingen der Manie im Rahmen einer Bipolaren Störung kann das Antipsychotikum in vielen Fällen abgesetzt werden, wenn das Phasenprophylaktikum weiter eingenommen wird. Reicht dies nicht aus, kann in einer zweiten Stufe eine Phasenprophylaxe mit zwei Phasenprophylaktika versucht werden, erst wenn auch dies scheitert, wird ein Antipsychotikum zusätzlich dauerhaft gegeben.
Bei schizoaffektiven Störungen wird die Phasenprophylaxe in der Regel gleich im ersten Schritt mit einer Kombination aus Antipsychotikum und Phasenprophylaktikum durchgeführt.
Depressionen mit psychotischen Symptomen
Die erste Wahl der Behandlung der Depression mit psychotischen Symptomen ist in vielen Fällen die EKT. Die zweite Wahl ist die Pharmakotherapie mit einer Kombination aus einem Antidepressivum und einem Antipsychotikum. Gibt man Risperidon in dieser Indikation, reichen in den meisten Fällen 0,5-2 mg aus. In der Gerontopsychiatrie reichen zumeist 0,25 bis 1 mg/Tag.
Aggressives Verhalten
Risperidon ist bei zwei klar eingegrenzten Patientengruppen zugelassen, um aggressives Verhalten zu reduzieren:
- Patienten mit Alzheimer Demenz nach Ausschöpfung anderer Therapiemöglichkeiten: In bestimmten Phasen der Alzheimer-Demenz kann es zu aggressivem Verhalten kommen, das zu erheblichen Problemen in der täglichen Versorgung der betroffenen Patienten führt. Wenn verhaltenstherapeutische Maßnahmen und angemessen eingesetzte Sedativa nicht ausreichend wirksam sind, kann ein Therapieversuch mit Risperidon angemessen sein. Das Ziel ist hier nicht Müdigkeit, sondern ein Abklingen des aggressiven Verhaltens. In der richtigen Kombination mit anderen Maßnahmen wird dieses Ziel nicht selten erreicht. Dabei muss man aber bedenken, dass Antipsychotika bei älteren Patienten die Gefahr von Schlaganfällen erhöhen können. Auch die Sturzneigung kann unter EPMS-lastigen Antipsychotika im Alter sehr zunehmen. Daher sollte man die Indikation für Risperidon in einer überlegten Abwägung gegen die möglichen Nebenwirkungen treffen und die erzielte Wirkung sowie die eingetretenen Nebenwirkungen gut beobachten.
- Geistig behinderte Kinder ab 5 Jahren und Jugendliche mit einer Verhaltensstörung: Auch hier ist es wichtig, zuvor alle verhaltensmodifizierenden Techniken versucht zu haben und auch hier ist der Grad zwischen erzielbarem Nutzen und möglichen Nebenwirkungen schmal. In bestimmten Fällen wirkt Risperidon in dieser Indikation gut gegen aggressive Verhaltensweisen, in anderen Fällen bewirkt es keine Verbesserung.
Dosierung
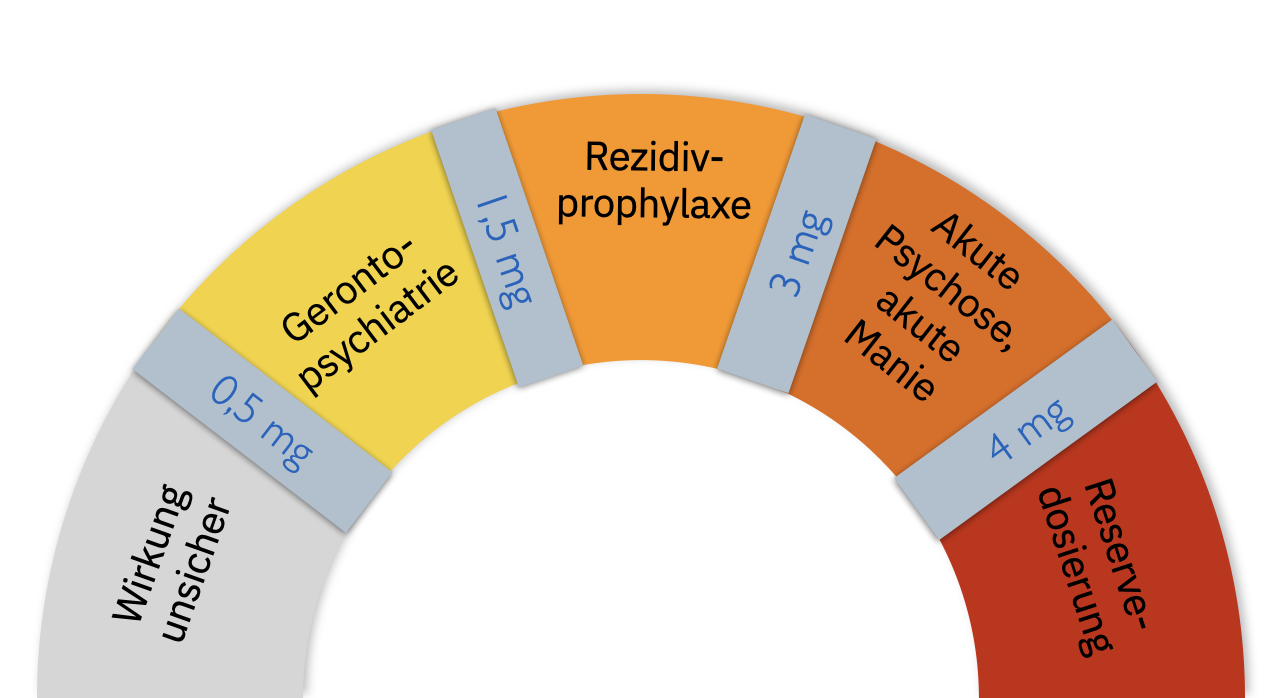
- akute Psychose, Manie: bis 2-4, maximal 6 mg/Tag
- Rezidivprophylaxe: 0,5–4 mg/Tag
- Depression mit psychotischen Symptomen: 0,5-2 mg/Tag
- Aversives Verhalten bei Demenz und aggressives Verhalten bei Jugendlichen mit Verhaltensstörung: 0,25–2 mg/Tag
- Gerontopsychiatrie: 0,25-2 mg/Tag meist ausreichend
- maximale Tagesdosis: 6 mg/Tag
Nebenwirkungen
EPMS
Die häufigste unerwünschte Wirkung von Risperidon sind EPMS (siehe Kapitel 4.6.1). Je nach Alter und persönlicher Disposition des Patienten können EPMS bei unterschiedlichen Dosierungen auftreten. Bei einer Dosis von 4 mg und mehr oder einem Blutspiegel von 40 ng und mehr treten EPMS allerdings sehr viel öfter auf. Im ersten Schritt sollte man die Dosis reduzieren. Dabei muss man wissen, dass sowohl beim Steigern der Dosis als auch beim Reduzieren der Dosis für einige Tage verstärkt EPMS auftreten können. Während EPMS bestehen, kann man versuchen, diese mit Biperiden zu lindern. Führt eine Reduktion der Dosis auch nach einigen Tagen nicht zu einem deutlichen Nachlassen der EPMS, ist im nächsten Schritt eine Umstellung auf ein in diesem Punkt verträglicheres Antipsychotikum zu erwägen, z.B. Olanzapin oder Ziprasidon.
Akathisie
Akathisie oder Sitzunruhe (siehe Kapitel 4.6.2) kann sehr quälend sein. Ist sie durch eine Dosisreduktion nicht in den Griff zu bekommen, wechselt man in der Regel auf ein anderes Medikament.
Hyperprolaktinämie
Wie alle D2-Antagonisten kann Risperidon eine Hyperprolaktinämie verursachen. Dies kann zum Milchfluß, einer Gynäkomastie beim Mann oder sexuellen Funktionsstörungen führen. Der Prolaktinwert im Blut ist bei Therapie mit D2-Antagonisten häufig erhöht. Wenn keine spezifischen Symptome vorliegen, muss aufgrund einer moderaten Laborwerterhöhung alleine nicht unbedingt das Medikament abgesetzt werden. Es ist aber wichtig, die Patienten über diese möglichen Nebenwirkungen aufzuklären, damit beim Auftreten von Symptomen eine Konsequenz gezogen werden kann.
Hypotonie
Aufgrund der Blockade von α-adrenergen Rezeptoren kann Risperidon insbesondere in der Aufdosierungsphase in einigen Fällen den Blutdruck senken.
Depressive Stimmungslage
Wie alle Dopamin-Antagonisten kann auch Risperidon bei manchen Patienten eine depressive Stimmungslage verursachen. Im Vordergrund stehen dabei am ehesten Antriebsstörungen, Motivationsmangel und ein Gefühl der Erschöpfung. Es können aber auch depressive Gedanken und Gefühle im engeren Sinne dazu kommen. In dieser Situation wechsele ich persönlich eher auf ein anderes Antipsychotikum wie z.B. Ziprasidon, als ein Antidepressivum zu ergänzen.
Risperidon in der Schwangerschaft und Stillzeit
Die Wahl von Psychopharmaka in Schwangerschaft und Stillzeit ist immer eine sehr individuelle Entscheidung und sollte immer nach gründlicher Recherche aktueller Datenbanken wie z.B. Embryotox erfolgen. Wenn die Indikation eindeutig ist und Risperidon bislang gut gewirkt hat, ist eine weitere Gabe in der Schwangerschaft unter engmaschigeren Blutspiegelkontrollen und möglichst niedriger Dosierung nach heutigem Wissensstand vertretbar.
Risperidon geht wie alle Psychopharmaka in die Muttermilch über, daher wird vom Stillen mit Muttermilch abgeraten.
Sinnvolle Laboruntersuchungen
- Vor Behandlungsbeginn und nach einem Monat: Blutbild, Elektrolyte, Kreatinin, GGT, Bilirubin, CK, INR, TSH, ß-HCG, EKG, Körpergewicht.
- Im ersten Jahr quartalsweise EKG, Routinelabor und Körpergewicht.
- Danach sind bei unkompliziertem Verlauf auch längere Kontrollintervalle üblich.
Mein persönliches Fazit
Risperidon ist zumeist gut und sicher wirksam. Daher ist es für mich oft das Antipsychotikum der 1. Wahl.
Es ist in Dosierungen bis 3 mg meist gut verträglich, es macht nicht müde und führt eher selten zu einer Gewichtszunahme.
Dosierungen von 5 und 6 mg/Tag verordne ich kaum noch, da diese öfter zu EPMS führen und meist nicht viel besser wirksam sind als 4 mg/Tag.
Hätte ich eine Psychose, würde ich mich mit Risperidon behandeln.
Copyright
Dieser Beitrag ist ein Auszug oder eine auszugsweise Vorabveröffentlichung des Werks „Psychopharmakotherapie griffbereit“ von Dr. Jan Dreher, © Georg Thieme Verlag KG. Die ausschließlichen Nutzungsrechte liegen beim Verlag. Bitte wenden Sie sich an permissions@thieme.de, sofern Sie den Beitrag weiterverwenden möchten.