Es gibt einen neuen Videokurs: Der Psychopharmaka-Videokurs. In über 7,5 Stunden Videocontent erkläre ich Dir die Psychopharmakologie, vom Praktiker, für den Praktiker. Mehr als 3 der 7,5 Stunden sind exklusiver Content im Kurs, 4,5 Stunden des Contents gibt es in anderer, längerer oder anders zusammen gestellter Form schon hier auf YouTube. Aber zusammen geleitet Dich der Kurs durch das gesamte Gebiet der Psychopharmakologie. Schau doch mal rein:
Neuroleptika
Neues Video online: Cariprazin
Depotneuroleptika
Das Kapitel „Depotneuroleptika“ in meinem Buch benötigte mal wieder eine Aktualisierung, da es mit TREVICTA® und OKEDI® zwei neue Depots auf dem Markt gibt, die ich noch nicht aufgeführt hatte. Ich habe es auch etwas vereinfacht. Wie es hier auf dem Blog guter Brauch ist, stelle ich das Kapitel hier zur Diskussion, mit der Bitte, Fehler, Fehlendes und Verbesserungsvorschläge in die Kommentare zu schreiben. Da der Text später im Buch erscheinen soll, steht er unter Copyright.
Einige der typischen Neuroleptika wie Haloperidol, Flupentixol oder Fluphenazin stehen schon seit Jahrzehnten auch als Depotpräparat zur Verfügung. Diese Darreichungsform galt lange Zeit für eine recht große Patientengruppe als besonders sicher und angemessen. Mit dem Aufkommen der Atypika änderte sich das Verhältnis aus Nutzen und Nachteilen, weil die Typika auch in der Depotform nebenwirkungsreicher sind als die Atypika. Mit Risperidon kam ein erstes Atypikum in Depotform auf den Markt, inzwischen stehen auch Olanzapin und Aripiprazol als Depot zur Verfügung. Paliperidon ist als monatlich oder als 3-monatlich zu gebendes Depot erhältlich. Risperidon steht in einer Formulierung zur Verfügung, die ohne Auftitrierung direkt nach der ersten Depotgabe den endgültigen Blutspiegel aufbaut.
Zum Einsatz eines Depotpräparates gibt es immer wieder unterschiedliche Einschätzungen. Wenn ein psychiatrischer Patient, der eine neuroleptische Medikation benötigt, diese immer wieder nach einer gewissen Zeit gegen ärztlichem Rat absetzt, kommt regelmäßig der Ruf nach einem Depotpräparat auf. Man muss jedoch bedenken, dass ein Patient, der sein Neuroleptikum nicht mehr nehmen möchte, es auch als Depot nicht nehmen wird. Depots haben große Vorteile, wenn jemand zwar alle 2–4 Wochen einen Arzt aufsucht, aber zwischenzeitlich eine Tabletteneinnahme nicht hinbekommt, etwa weil er obdachlos ist und das Depot für ihn praktischer ist. Sie sind auch vorteilhaft, wenn ein Patient die Medikation zwar möchte, aber die Tabletteneinnahme ihm zu lästig oder zu kompliziert ist oder er sie häufig vergisst.
Man muss auf der anderen Seite beachten, dass es bei nicht steril applizierten Depotinjektionen zu einem Spritzenabszess kommen kann, der die Gesundheit erheblich gefährden kann und manchmal zu einer großen Narbe führt. Das passiert mit Tabletten nicht. Das Risiko eines Spritzenabszesses muss einem klaren Vorteil der Depotmedikation gegenübergestellt werden.
Wenn ein Patient ein Neuroleptikum nicht nehmen möchte und es keine gesetzliche Grundlage wie eine Bewährungsauflage gibt, dann kann er auch eine Depotmedikation jederzeit absetzen. Immerhin – man sieht es frühzeitig.
Umstellung einer oralen Gabe auf ein Depot
Bevor man ein Neuroleptikum als Depot gibt, muss man sicherstellen, dass dessen Wirkstoff auch vertragen wird. Es wäre fatal, wenn man eine Substanz als Depot verabreicht, und diese dann starke EPMS, starke Akathisie oder eine andere Nebenwirkung verursacht, denn diese Nebenwirkung würde ja wochenlang bestehen bleiben. Daher muss der Wirkstoff zuerst immer in kurzwirksamer Form, also in der Regel als Tablette gegeben werden. Bei guter Verträglichkeit kann dann auf ein Depot umgestellt werden.
Allerdings führt die erste Gabe bei den meisten Depotpräparaten eben gerade noch nicht zu einem ausreichenden Blutspiegel. Nur Risperidon ISM (OKEDI®) hat eine Pharmakodynamik, die direkt nach der ersten Gabe ausreichende Blutspiegel erzeugt. Bei den anderen Präparaten gibt man eine loading-dose wie bei Xeplion® oder gibt über zwei bis drei Depotintervalle parallel den gleichen Wirkstoff noch in Tablettenform dazu.
Dann stellt sich die Frage nach der Umrechnung einer bisherigen oralen Dosis in eine Depotdosis. Es gibt keine einfache Formel, um die oral gegebene Dosis eines Neuroleptikums in eine Depotdosis umzurechnen. Zur Orientierung habe ich aus den Fachinformationen und teilweise aus meiner klinischen Erfahrung in Tabelle 4.3. vergleichbare orale Dosierungen und Depot-Dosierungen aufgeführt. Im Einzelfall können andere Dosierungen erforderlich sein. Der Tabelle ist auch zu entnehmen, in welchen Dosierungen das jeweilige Depot vorliegt und in welchen Intervallen es zu geben ist.
| Dosis in Worten | Dosis in Tablettenform | Depotdosis |
|---|---|---|
| Haloperidol (z.B. Haldol®) | ||
| niedrig | 2-0-2 mg | 40 mg alle 4 Wochen |
| mittel | 4-0-4 mg | 80 mg alle 4 Wochen |
| hoch | 6-0-6 mg | 120 mg alle 4 Wochen |
| Flupentixol (z.B. Fluanxol®) | ||
| niedrig | 4-0-0 mg | 20 mg alle 2 Wochen |
| mittel | 10-0-0 mg | 50 mg alle 2 Wochen |
| hoch | 10-10-0 mg | 100 mg alle 2 Wochen |
| Fluphenazin (z.B. Lyogen®) | ||
| niedrig | 2-0-3 mg | 25 mg alle 2 Wochen |
| mittel | 5-0-5 mg | 50 mg alle 2 Wochen |
| hoch | 10-0-10 mg | 100 mg alle 2 Wochen |
| Risperidon mit 2-wöchiger Gabe (z.B. Risperdal Consta®) | ||
| niedrig | 0-0-2,5 mg | 25 mg alle 2 Wochen |
| mittel | 0-0-4 mg | 37,5 mg alle 2 Wochen |
| hoch | 0-0-5 mg | 50 mg alle 2 Wochen |
| Paliperidon mit 4-wöchiger Gabe (Xeplion®) | ||
| Xeplion-Einstellung auf jede Dosis immer so beginnen: Tag 1: 150 mg deltoidal, Tag 8: 100 mg deltoidal, danach: | ||
| niedrig | 3–0–0 mg | 50 mg alle 4 Wochen |
| mittel | 6-0-0 mg | 75 mg alle 4 Wochen |
| hoch | 6-0-3 mg | 100 mg alle 4 Wochen |
| Paliperidon mit 12-wöchiger Gabe (z.B. TREVICTA®) | ||
| Nach viermonatiger Gabe von Xeplion® soll auf die 3,5 fache Dosis TREVICTA® umgestellt werden. | ||
| niedrig | 50 mg Xeplion® alle vier Wochen | 175 mg TREVICTA® mg alle 12 Wochen |
| mittel | 75 mg Xeplion® alle vier Wochen | 263 mg TREVICTA® mg alle 12 Wochen |
| hoch | 100 mg Xeplion® alle vier Wochen | 350 mg TREVICTA® mg alle 12 Wochen |
| sehr hoch | 150 mg Xeplion® alle vier Wochen | 525 mg TREVICTA® mg alle 12 Wochen |
| Risperidon ISM (z.B. OKEDI®) | ||
| OKEDI® kann gegeben werden, wenn sichergestellt ist, dass Risperidon vertragen wird. Es baut den Wirkstoffspiegel direkt mit der ersten Depot-Gabe auf. | ||
| niedrig | 3-0-0 mg | 75 mg alle 4 Wochen |
| mittel | 4-0-0 mg | 100 mg alle 4 Wochen |
| Aripiprazol (z.B. Abilify Maintena®) | ||
| mittel | 15-0-0 mg | 300 mg alle 4 Wochen |
| hoch | 20-0-0 mg | 400 mg alle 4 Wochen |
| Olanzapin (z.B. ZypAdhera®) | ||
| niedrig | 0-0-10 mg | 210 mg alle 2 Wochen oder 405 mg alle 4 Wochen für 8 Wochen. Danach 150 mg alle 2 Wochen oder 300 mg alle 4 Wochen. |
| mittel | 0-0-15 mg | 300 mg alle 2 Wochen für 8 Wochen. Danach 210 mg alle 2 Wochen oder 405 mg alle 4 Wochen. |
| hoch | 0-0-20 mg | 300 mg alle 2 Wochen. |
Copyright
Dieser Beitrag ist ein Auszug beziehungsweise eine auszugsweise Vorabveröffentlichung des Werks „Psychopharmakotherapie griffbereit“ von Dr. Jan Dreher, © Georg Thieme Verlag KG. Die ausschließlichen Nutzungsrechte liegen beim Verlag. Bitte wenden Sie sich an permissions@thieme.de, sofern Sie den Beitrag weiterverwenden möchten.
Mein neues Video Eine ehrliche Aufklärung über Neuroleptika ist online
In diesem Video beschreibe ich, welche Nebenwirkungen unter Neuroleptika häufig vorkommen. Ich beginne mit einem Fallbeispiel, dass zeigt, dass Neuroleptika gut gegen Psychosen wirken, aber oft aufgrund von Nebenwirkungen abgesetzt werden. Ich erkläre die Einteilung der Neuroleptika in niedrigpotente Neuroleptika und hochpotente Neuroleptika. Hochpotente Neuroleptika sollte man besser Antipsychotika nennen, da sie die psychotische Symptome gut behandeln können. Die hochpotenten Antipsychotika werden noch einmal in typische und atypische Neuroleptika unterteilt. Ich erkläre dann die vier wichtigsten dopaminergen Bahnen im Gehirn. Bei der Therapie mit Neuroleptika werden diese Bahnen in ihrer Aktivität gebremst.
Dies führt zu typischen Nebenwirkungen:
Das Mesolimbische System
- Dies ist das System, das wohl bei der Psychose am ehesten überhitzt ist. Beim Gesunden ist es für Freude, Lust und Motivation da. Wenn in diesem System Dopamin ausgeschüttet wird, dann weiß der Mensch: Hier passiert gleich etwas Wichtiges, hier lohnt es sich, aufzupassen und dranzubleiben.
- Wenn man dieses System mit Antipsychotika zu stark drosselt, ergeben sich daraus oft Lustlosigkeit und Interessenverlust.
Das Nigrostriatale System
- Dieses System ist beim Gesunden für Bewegungen zuständig.
- Eine bekannte Krankheit, bei der zu wenig Dopamin in diesem System zur Verfügung steht, ist der M. Parkinson.
- Die gleichen Beschwerden wie beim Parkinson treten auf, wenn antipsychotische Medikamente das nigrostriatale System zu stark drosseln, es entsteht ein medikamentös verursachter Parkinsonismus. Die Patienten gehen mit steifen Armen und Beinen, man sagt „wie ein Teddybär“, sie zittern, die Mimik ist reduziert und spontane Bewegungen fallen schwer.
Das Mesocortikale System
- Ist beim Gesunden für Denken, Gefühle und Motivation zuständig.
- Wird es durch Antipsychotika zu stark gedämpft, können Antriebslosigkeit und Affektverflachung entstehen. Die Patienten „kommen einfach nicht mehr aus dem Quark“ und verlieren das Interesse an allem. Nichts macht mehr richtig Spaß und daher scheint es sich für nichts mehr zu lohnen, sich aufzuraffen.
Das Tuberoinfundibuläre System
- Regelt beim Gesunden die Freisetzung des Hormons Prolactin. Das Hormon Prolactin führt zur Milchproduktion in den Brustdrüsen. Dies ist bei Frauen in der Stillzeit ja auch sinnvoll.
- Dopamin ist das „Prolactin inhibitin factor“ eine Dopaminblockade durch Antipsychotika führt also zu einer Überproduktion von Prolactin, einer Hyperprolactinämie.
- Wenn zu viel Prolactin im Blut ist kommt es bei Frauen und Männern zu einem Milchfluß. Es fließt also sowohl bei Frauen als auch bei Männern aus den bei Männern ja auch angelegten Brustdrüsen Milch. Darüber hinaus kann es durch einen zu hohen Prolactinspiegel zu sexuellen Funktionsstörungen kommen.
Dann gehe ich kurz auf einige spezifische Nebenwirkungen bestimmter Neuroleptika ein, wie z.B. QTc-Zeit-Verlängerungen, das metabolische Syndrom oder die Agranulozytose. Schließlich nenne ich einige Vorgehensweisen, die helfen können, Nebenwirkungen zu verhindern und spreche darüber, was man tun kann, wenn dennoch Nebenwirkungen aufgetreten sind.
Quellen
https://commons.wikimedia.org/wiki/File:Dopaminergic_pathways.svg
Wem meine Grafik gefällt, der darf sie gerne weiterverwenden:

Video „Blutspiegel bei Depot-Neuroleptika?“
Hörerin Julia hat gefragt, der PSychCast antwortet!
Welches Neuroleptikum gebe ich wem?
Welches Neuroleptikum gebe ich eigentlich wem? In diesem Beitrag erfährst du, welche Überlegungen ich als Psychiater anstelle, wenn ich entscheide, welches Neuroleptikum ich wem empfehle. Wenn Du den Beitrag gerne als Video sehen möchtest, click einfach auf diesen Link. Zum Nachlesen habe ich die wichtigsten Eckpunkte hier noch einmal aufgeschrieben.
Einleitung
Die Psychose ist keine seltene Erkrankung; etwa 0,5-1% der Bevölkerung entwickeln irgendwann in ihrem Leben einmal eine Psychose. Meistens fällt der Erkrankungsbeginn in die Zeit zwischen dem 18.ten und 25.ten Lebensjahr; er kann aber auch später liegen. Ursachen können eine genetische Veranlagung sein, aber auch Drogen, insbesondere Amphetamine, Cocain und THC können die Entstehung einer Psychose begünstigen. Und es gibt noch einige andere Krankheitsbilder, die mit psychotischen Symptomen einhergehen, darunter das Delir, wahnhafte Depressionen, akute psychotische Zustände bei Drogenintoxikationen und noch einige wenige andere.
Diese Krankheiten sind in der Regel gut behandelbar. Der Schlüssel zur Behandlung liegt in der Gabe der richtigen Medikamente.
Begriffsbestimmung
Ich habe bis jetzt den Begriff Neuroleptika benutzt, weil er am bekanntesten und gebräuchlichsten ist. Der Begriff Neuroleptika ist allerdings ein Überbegriff.
- Zu den Neuroleptika zählen die sogenannten hochpotenten Neuroleptika wie Haloperidol, Risperidon und andere Medikamente, die gegen psychotische Symptome wirken. Diese Medikamente nennt man präziser Antipsychotika, weil sie gegen psychotische Symptome wirken, also gegen Wahn und Halluzinationen.
- Der zweite Teil der Neuroleptika sind die sogenannten niederpotenten Neuroleptika wie Promethazin, Pipamperon und andere, die kaum gegen psychotische Symptome wirken, aber sedieren. Diese Gruppe nennt man präziser Sedativa us der Gruppe der Neuroleptika.
In diesem Video gehe ich auf die Auswahl des passenden Antipsychotikums ein, und verwende ab jetzt auch diesen Begriff.
Wem empfehle ich jetzt welches Antipsychotikum?
Nehmen wir zum Beispiel einen jungen Mann, der an einer Schizophrenie erkrankt, keine anderen Krankheiten hat und mich nach einer Medikation fragt. Für mich als Psychiater ist das eine typische Fragestellung, und es gibt einige typische Situationen, die ich hier berichten kann. Natürlich ist dies nicht der einzig richtige Weg.
Nehmen wir also an, in meine Behandlung kommt ein sonst gesunder Patient mit einer Psychose. Ich entscheide mich, dass er ein Neuroleptikum braucht. Das bespreche ich mit ihm und er stimmt zu. Nun stellt sich die Frage: Welches Neuroleptikum empfehle beziehungsweise verordne ich? Es gibt keine ganz einfache Faustformel, nach der ich für einen bestimmten Patienten ein Neuroleptikum auswähle, aber ich habe ein typisches Vorgehen, das ich häufig anwende.
Auswahl nach Wirkung oder nach Nebenwirkungen?
Wenn ich ein Medikament auswähle, dann denke ich zunächst einmal an die angestrebte Wirkung. Bei Antipsychotika ist das ganz einfach die antipsychotische Wirkung. Und tatsächlich unterscheiden sich die verschiedenen Antipsychotika auch ein wenig in ihrer Wirkstärke. Eine floride Psychose mit akuten Gefährdungsaspekten mit dem nur mittelstark antipsychotisch wirksamen Quetiapin zu behandeln erfordert Geduld und Mut…
Aber letztlich sind die verschiedenen Antipsychotika in ihrer antipsychotischen Wirkung recht ähnlich. Praktisch muss man daher mindestens genau so die möglichen Nebenwirkungen in den Blick nehmen. Aber dazu gleich mehr. Fangen wir mal mit einem unkomplizierten Fall an!
Der erfolgreich vorbehandelte Patient
Auf meine Fragen: „Haben Sie schon einmal in einer früheren Krankheitsphase ein Neuroleptikum erhalten? Hat es gut gewirkt? Haben Sie es gut vertragen?“, antwortet er jeweils mit „Ja“, d. h. ein bestimmtes Präparat hat schon einmal gut gewirkt und wurde gut vertragen. Dann empfehle ich genau dieses Medikament wieder. Ich frage, welche Symptomatik damals bestanden hat, wie stark sie war und welche Dosis des Präparates in welcher Zeit geholfen hat. Ich mache mir ein Bild davon, wie stark die Symptomatik jetzt ist und empfehle eine passende Dosis.
Der bislang unbehandelte Patient mit einer eindeutig psychotischen Symptomatik
Wenn bislang noch nie ein Neuroleptikum verordnet wurde, empfehle ich selbst in der Regel in der ersten Stufe Risperidon. Das ist natürlich nicht der Weisheit letzter Schluss, und andere Psychiater gehen hier anders vor, aber ich stelle hier ja meinen eigenen Weg vor.
Es wirkt schnell und verlässlich. Es macht nicht müde und es verursacht in der Regel keine Gewichtszunahme. In Dosierungen bis 4 mg/Tag ist es meist gut verträglich und macht bei vielen Patienten keine EPMS (S.113). In höheren Dosierungen kann es EPMS verursachen.
Risperidon hat sich als ungeeignet erwiesen: Olanzapin
Wenn Risperidon nicht ausreichend geholfen hat oder nicht vertragen wurde und der Patient nicht adipös ist, empfehle ich in der zweiten Stufe in der Regel Olanzapin. Es wirkt ebenso sicher, verlässlich und zügig wie Risperidon und wird ebenfalls zumeist gut vertragen. Es kann aber eine deutliche Gewichtszunahme verursachen. Darüber kläre ich den Patienten sehr eindeutig auf. Lehnt er das Präparat ab, empfehle ich ein anderes. Ich lasse die Patienten vor Beginn der Behandlung mit Olanzapin wiegen. Treten eine Gewichtszunahme von mehr als 3 kg oder wiederholte Heißhungerattacken auf, empfehle ich, das Präparat zu wechseln.
Risperidon und Olanzapin haben sich als ungeeignet erwiesen: Amisulprid
Wenn Risperidon in Stufe eins wegen mangelnder Wirksamkeit und nicht wegen EPMS das Feld räumen musste und in Stufe zwei Olanzapin nicht geeignet war, dann versuche ich in der dritten Stufe Amisulprid. Wenn Risperidon wegen EPMS ausschied, überspringe ich diesen Schritt.
Risperidon, Olanzapin und Amisulprid waren ungeeignet: Aripiprazol, Ziprasidon und Quetiapin
In der vierten Stufe muss ich ein Antipsychotika auswählen, das ggf. etwas weniger wirkstark als Risperidon, Olanzapin und Amisulprid, aber vielleicht besser verträglich ist. Es kommen nun Aripiprazol, Ziprasidon und Quetiapin in Betracht. Ich verordne in dieser Reihenfolge. Aripiprazol führt häufig zu Akathisie, ich setze es dann zumeist sofort und ohne zu warten ab. Ziprasidon und Quetiapin werden in der Regel sehr gut vertragen, hier stellt sich eher die Frage der ausreichenden Wirksamkeit.
Die Negativsymptomatik steht im Vordergrund: Cariprazin
Cariprazin hat eine dem Risperidon vergleichbare Wirkung auf die Positivsymptomatik, hat aber in den bisherigen Studien eine Überlegenheit in der Wirkung auf Negativsymptomatik.
Eine Monotherapie war ohne Erfolg: Kombinationstherapie
Funktioniert keines der bislang gewählten Antipsychotika in Monotherapie, wähle ich geleitet von den Nebenwirkungen der bisherigen Versuche eine Kombinationstherapie aus zwei gut verträglichen, aber in Monotherapie nicht ausreichend wirksamen Antipsychotika aus und gebe beide in einer mittleren Dosis. Dabei unterteile ich die Antipsychotika nach ihren Nebenwirkungen in unterschiedliche Gruppen und meide die Gruppe, deren Nebenwirkung bislang am problematischsten war:
Fünf Gruppen von Antipsychotika
- EPMS-Gefahr: Haloperidol, Amisulprid, Risperidon, Cariprazin
- Gewichtszunahme-Gefahr: Olanzapin, Quetiapin
- Akathisie-Gefahr: Aripiprazol
- Möglicherweise schwache Wirkung, dafür bessere Verträglichkeit: Ziprasidon
- Reserveantipsychotika: Sertindol, Clozapin
Alle oben genannten Stufen waren erfolglos: Sertindol
Waren die bisherigen Wirkstoffe und eine Zweifachkombination erfolglos, dann probiere ich es mit Sertindol. Zu Sertindol sind besondere Hinweise zu beachten, da es in besonders hohem Maße die QTc-Zeit verlängern kann. Es ist daher ein Neuroleptikum der zweiten Wahl.
Sertindol war auch erfolglos: Clozapin
Wenn Sertindol auch nicht gewirkt hat oder wenn die Schwere der Erkrankung dies schon früher gebietet, kann es an der Zeit sein, sich für das nebenwirkungsreichere, aber eben auch sehr wirksame Clozapin zu entscheiden. Eine besonders ausführliche Aufklärung ist erforderlich. In der S 3-Behandlungsleitlinie „Schizophrenie“ wird der Einsatz von Clozapin deutlich früher in Betracht gezogen. Da Clozapin aber regelmäßig starke Nebenwirkungen verursacht, setze ich es nach Möglichkeit erst spät ein.
Behandlung akuter cocaininduzierter psychotischer Zustände
Cocain ist stark und selektiv dopaminagonistisch. Amisulprid ist stark und selektiv dopaminantagonistisch. Daher behandele ich akute psychotische Zustände nach Cocainkonsum mit Amisulprid und einem Benzodiazepin.
Delir mit psychotischen Symptomen
Ein lebensbedrohliches Delir, egal welcher Genese (Alkoholentzug, Benzodiazepinentzug, …) braucht eine wirkungsvolle und schnelle Neurolepsie. Ich gebe inzwischen meistens Risperidon, bei mangelnder Wirkung steige ich auf Haloperidol oder Olanzapin um. Ältere Patienten mit Delir behandele ich auch manchmal mit Quetiapin. Zur Behandlung des Delirs habe ich ein eigenes Video gemacht, das ich hier oben rechts verlinkt habe.
Rezidivprophylaxe bei asymptomatischem Patienten
Mit großer Sicherheit wirkt das Neuroleptikum, das die psychotische Episode beendet hat. Bei der Rezidivprophylaxe sind aber Nebenwirkungen noch viel weniger akzeptabel als in der Akuttherapie. Bei Nebenwirkungen wechsele ich daher noch niederschwelliger auf ein Ausweichpräparat.
Auswahl eines Depotpräparates
Wenn der Patient unter den zuvor verordneten Medikamenten keine Probleme mit EPMS hatte, mache ich in der Regel zunächst einen Versuch mit Flupentixol (Fluanxol ® ). Zur Prüfung der Verträglichkeit gebe ich es zunächst oral. Wird dies vertragen, gebe ich eine milde Dosis Fluanxol Depot, etwa 40-60 mg alle 2 Wochen. Alternativ gebe ich Risperidon (Risperdal ® Consta ® ) oder Paliperidon (Xeplion ® ) als Depotpräparat. Treten hierunter EPMS auf, gebe ich Olanzapin als Depotpräparat (ZypAdhera ® ).
Wenn ich selbst ein Antipsychotikum bräuchte
Wenn ich selbst ein Neuroleptikum bräuchte, würde ich mich für Risperidon entscheiden. Möglicherweise auch Cariprazin.
Das ist natürlich eine Vereinfachung… 🙂
Ich weise darauf hin, dass bei jedem einzelnen Patienten noch viele weitere Aspekte eine Rolle spielen können, die über das von mir beschriebene Vorgehen hinausgehen. Dies Vorgehen ist ja eine Vereinfachung und ein erster Einstieg.
Wenn ihr mehr über Psychopharmakotherapie wissen wollt, und euch eine Erklärung in verständlicher Sprache wichtig ist, dann guckt euch auch mal mein Buch Psychopharmakotherapie griffbereit an.
Copyright
Dieser Beitrag ist ein Auszug beziehungsweise eine auszugsweise Vorabveröffentlichung des Werks „Psychopharmakotherapie griffbereit“ von Dr. Jan Dreher, © Georg Thieme Verlag KG. Die ausschließlichen Nutzungsrechte liegen beim Verlag. Bitte wenden Sie sich an permissions@thieme.de, sofern Sie den Beitrag weiterverwenden möchten.
Vereinfachte Nebenwirkungsprofile ausgewählter Antipsychotika

Ich habe mich – aus Gründen – hier mal an einer Grafik versucht, die das Nebenwirkungsprofil ausgewählter Antipsychotika vereinfachend aber übersichtlich darstellt. Die Kunst bei dieser Grafik läge darin, zu vermitteln, wo der Hase bei jedem einzelnen Medikament im Pfeffer liegt, wohl wissend, dass dies alles eine Vereinfachung ist.
Wie sieht die Grafik für euch aus? Kann man damit was anfangen? Ist das ganze Konzept zu vereinfachend? Muss ein bestimmtes Medikament in eine Richtung verrückt werden?
Schreibt mir eure Ideen dazu gerne in die Kommentare! #followerpower
Wie rechne ich die Dosis eines Neuroleptikums auf ein anderes um?

Wenn man ein Medikament aus einer bestimmten Gruppe auf ein anderes Medikament aus derselben Gruppe umstellen möchte, dann ist es ganz hilfreich, eine Vorstellung davon zu haben, welche Dosierungen sich in etwa entsprechen. Natürlich kann man die Dosierungen nicht einfach umrechnen, denn jede Substanz hat doch etwas andere Hauptwirkungen und oft erheblich unterschiedliche Nebenwirkungen. Dennoch ist es hilfreich, einen Anhaltspunkt zu haben, in welcher Größenordnung sich die neue Dosis so bewegt.
Es gibt verschiedene Arten, an so eine Umrechnungstabelle zu kommen. Die klassische Variante ist die von Davis 1974 angewendete: Man nimmt sich alle verfügbaren Studien zu Medikamenten einer Gruppe, in der die Studienärzte nicht wussten, welches Medikament sie gaben, aber die Dosis nach der klinischen Wirkstärke anpassen konnten. Dann nimmt man den Mittelwert der jeweils gegebenen Dosierungen und geht davon aus, dass diese Mittelwerte vergleichbar sind. In einer ausgezeichneten Arbeit hat Leucht dieses Vorgehen 2015 für atypische Antipsychotika durchgeführt1. Das PDF der Studie ist kostenlos hier zu laden.
Cariprazin wurde in dieser Studie nicht untersucht. Die Äquivalenzwerte für Cariprazin habe ich daher aus meiner eigenen klinischen Erfahrung geschätzt und mich an dieser Studie2 angelehnt.
Ich habe auf diesem Blog bereits meine eigene Umrechnungstabelle für Opiate und meine eigene Umrechnungstabelle für Antidepressiva veröffentlicht. Das Bild oben zeigt die Tabelle, die sich aus der Studie von Leucht für die Gruppe der Antipsychotika ergeben. Ich habe deutsche Handelsnamen eingesetzt, die resultierenden Dosierungen auf für die nächste für dieses Präparat übliche Dosis gerundet und diejenigen Tabellenfelder leer gelassen, die Dosierungen enthalten hätten, die für dieses Präparat in Deutschland nicht zugelassen sind.
Wer sich ein eigenes Bild über meine Rundungen und Vereinfachungen machen möchte, der findet die Tabelle mit den präzise berechneten Werten, die ich als Ausgangswerte für die Tabelle oben genommen habe, hier:

Meiner persönlichen Einschätzung nach ist die Tabelle oben realistisch und gut geeignet, einen Anhaltspunkt dafür zu geben, welche Dosis eines Antipsychotikums welcher Dosis eines anderen Antipsychotikums entspricht.
Disclaimer
Auch zu dieser Tabelle möchte ich sagen, dass die hier angegebenen Dosierungen nicht ungeprüft übernommen werden dürfen. Die Verschreibung obliegt der Verantwortung des verschreibenden Arztes, der anhand der Fachinformationen, der individuellen Situation des Patienten und aller anderen relevanten Faktoren eine Wahl treffen muss.
Copyright
Dieser Beitrag ist ein Auszug beziehungsweise eine auszugsweise Vorabveröffentlichung des Werks „Psychopharmakotherapie griffbereit“ von Dr. Jan Dreher, © Georg Thieme Verlag KG. Die ausschließlichen Nutzungsrechte liegen beim Verlag. Bitte wenden Sie sich an permissions@thieme.de, sofern Sie den Beitrag weiterverwenden möchten.
- 1 Leucht S, Samara M, Heres S, Patel MX, Furukawa T, Cipriani A, Geddes J, Davis JM. Dose Equivalents for Second-Generation Antipsychotic Drugs: The Classical Mean Dose Method. Schizophr Bull 2015; 41: 1397–1402 Im Internet: https://academic.oup.com/schizophreniabulletin/article/41/6/1397/2526028 ↩︎
- 1 Németh G, Laszlovszky I, Czobor P, Szalai E, Szatmári B, Harsányi J, Barabássy Á, Debelle M, Durgam S, Bitter I, Marder S, Fleischhacker WW. Cariprazine versus risperidone monotherapy for treatment of predominant negative symptoms in patients with schizophrenia: a randomised, double-blind, controlled trial. Lancet 2017; 389: 1103–1113 Im Internet: https://linkinghub.elsevier.com/retrieve/pii/S0140673617300600 ↩︎
Darf ich mit Medikamenten Auto fahren?
In diesem Video erkläre ich, welche Überlegungen ich anstelle, wenn ich einen Patienten berate, ob er trotz psychiatrischer Erkrankung und Medikation wieder Auto fahren darf.
Vertragen sich meine Psychopharmaka mit Alkohol?
Die meisten Ärzte sagen dazu: „Nein, verzichten sie am Besten ganz auf Alkohol, wenn sie Medikamente einnehmen“. Das ist ja auch ein gut gemeinter Rat. Aber die Wahrheit ist etwas differenzierter. Wenn du wirklich wissen willst, welche Wechselwirkungen zwischen Alkohol und bestimmten Psychopharmaka typischerweise auftreten können, und welche Überlegung ich anstelle, wenn ich diese Frage beantworte, dann guck dir dieses Video an…
Moderne Behandlung des Delirs: Ein how-to-Video für Praktiker
Im Delir gebe ich doch immer Haldol und Diazepam, oder? Warum das fast immer falsch ist, und wie ich es nach dem aktuellen Stand der Wissenschaft richtig machen kann, erkläre ich euch in diesem Video.
Video: Blutspiegel in der Psychiatrie
Und es geht weiter mit einem neuen YouTube Video, diesmal erkläre ich, was es mit den Blutspiegeln der Medikamente in der Psychiatrie auf sich hat, in welchen Situationen und zu welchem Zeitpunkt man sie bestimmt, woran man sich orientiert und zeige euch an einem praktischen Beispiel, wie man einen Blutspiegel richtig interpretiert. Das Video findet ihr hier.
Die empfohlenen Blutspiegelbereiche der verschiedenen Wirkstoffgruppen sowie die Quellenangaben findest Du hier. Mein Buch Psychopharmakotherapie griffbereit findest Du hier.
Welche Kombinationen von Neuroleptika bieten sich an?
Welche Kombinationen von Neuroleptika bieten sich an?
Im ersten Schritt einer antipsychotischen Therapie ist die Monotherapie mit einem Neuroleptikum anzustreben. Bleibt diese erfolglos oder wird sie nicht vertragen, soll man im nächsten Schritt auf ein anderes Neuroleptikum in Monotherapie wechseln. Bleibt auch dies erfolglos, kann man entweder ein drittes Neuroleptikum in Monotherapie geben, oder eine Kombination von zwei Neuroleptika versuchen.
Die Auswahl des richtigen Neuroleptikums ist eine komplexe Angelegenheit. In die Wahl fließen verschiedene Aspekte ein, darunter Vorbehandlungen des Patienten und die Erfahrungen hiermit, individuelle Faktoren wie die Schwere und Akuität der Symptomatik, das zu erwartende Nebenwirkungsprofil des Medikamentes und auch persönliche Präferenzen des Behandlers.
Welches Neuroleptikum ich zu Beginn einer Behandlung nach welcher Überlegung einsetze, habe ich in meinem Buch Psychopharmakotherapie griffbereit und im Blog hier einmal beschrieben.
Aber nach welcher Überlegung wähle ich aus, welche Neuroleptika man gut miteinander kombinieren kann und bei welchen die Kombination kaum zusätzlichen Nutzen verspricht?
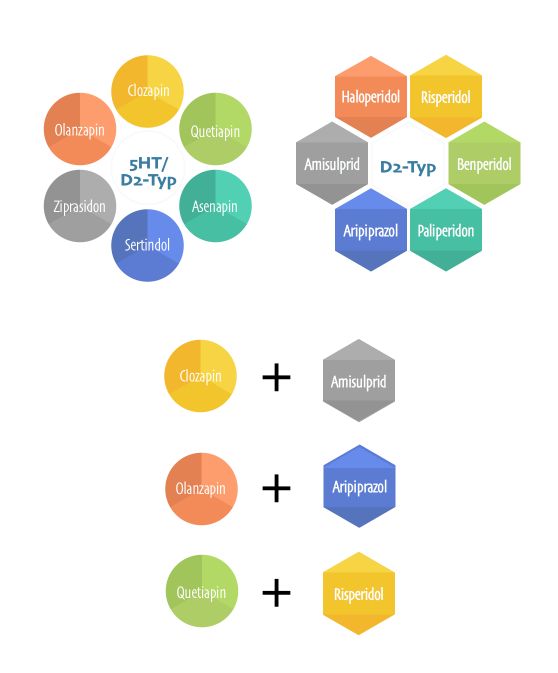
Um ehrlich zu sein: Für die Frage nach sinnvollen Kombinationen zweier Neuroleptika habe ich im wesentlichen ein Modell im Kopf: Ich unterteile für mich die Neuroleptika in zwei Gruppen.
- Die D2-affine Gruppe: In diese Gruppe gehören für mich alle Neuroleptika, deren Wirkung primär über eine Blockade des Dopamin-D2-Rezeptors zustande kommt. Dazu gehören alle alten, typischen Neuroleptika, wie Haloperidol und Benperidol. Ich zähle auch die atypischen Neuroleptika Risperidon, Amisulprid und Aripiprazol dazu, die in niedrigen Dosierungen kaum EPMS verursachen, die aber doch zu einem erheblichen Teil ihre Wirkung am D2-Rezeptor entfalten.
- Die 5HT / D2-affine Gruppe: In diese gehören für mich alle Neuroleptika, die sowohl den D2-Rezeptor als auch in relevantem Ausmaß den 5HT-2a-Rezeptor blockieren. Diese Neuroleptika gehören alle zur Gruppe der atypischen Neuroleptika, weil sie in üblichen Dosierungen keine EMPS verursachen. Dazu zählen für mich Clozapin, Olanzapin, Quetiapin, Sertindol, Ziprasidon und Asenapin.
Diese Gruppenzuordnung ist weder pharmakologisch ganz sauber, noch wissenschaftlich fundiert, noch Expertenkonsens. Egal. Wenn ich von einem Neuroleptikum wegen mangelnder Wirksamkeit oder zu großen Nebenwirkungen auf ein anderes wechsel, dann wechsel ich in der Regel auch zwischen diesen beiden Gruppen. Und wenn ich zwei Neuroleptika miteinander kombiniere, dann kombiniere ich in aller Regel eines aus der einen und eines aus der anderen Gruppe. Gute und bewährte Kombinationen sind zum Beispiel Amisulprid aus Gruppe 1 und Clozapin aus Gruppe 2. Ich habe da mal dieses hübsche Schaubild gemacht. Was haltet ihr von diesem Vorgehen?
Die Verzweiflung des Therapeuten ist keine Indikation für ein Neuroleptikum

Damit wir uns nicht falsch verstehen: Psychotische Zustände aller Art sind natürlich eine klare Indikation für ein Neuroleptikum, und ich bin froh und dankbar, dass es zur Behandlung von Psychosen, von wahnhaften Depressionen, Delirien und anderen Erkrankungen mit psychotischen Symptomen Neuroleptika gibt und ich verschreibe Neuroleptika in dieser Indikation natürlich.
Und es gibt auch Indikationen jenseits eindeutig psychotischer Symptome für den Einsatz von Neuroleptika. So haben sie ihre Existenzberechtigung in der Therapie von ganz bestimmten Impulskontrollstörungen. Und ja, sie können bei Gedankengrübeln im Rahmen schwerer Depressionen eine auflockernde Wirkung haben.
Aber so wirksam sie bei psychotischen Erkrankungen sind; Wundermittel sind die Neuroleptika nun unzweifelhaft auch nicht. Es gibt viele Situationen, in denen man sich ein wirkstarkes Medikament wünscht, aber keines zur Verfügung hat. Dann hilft aber auch der Griff zum Neuroleptikum nichts.
Typische Beispiele sind:
- Borderline-PatientInnen ohne psychotische Symptome erhalten oft ein mittelpotentes Neuroleptikum. Dies sediert und wird daher von den PatientInnen selbst nicht selten als angenehm empfunden. Für die über die Sedierung hinausgehende neuroleptische Komponente gibt es aber keine Indikation und meiner Einschätzung nach bewirkt sie auch keine Abnahme von Anspannung, Dissoziation, selbstverletzendem Verhalten oder anderen Borderline-typischen Symptomen. So schön das auch wäre.
- Neuroleptika bewirken auch keine Stabilisierung der Stimmung über den Verlauf eines Tages. Das können nicht einmal die irreführend als „Stimmungsstabiliserer“ benannten Phasenprophylaktika. Und Neuroleptika schon gar nicht.
- Ich weiß, dass Quetiapin Zulassungen als Phasenprophylaktikum und zur Augmentation (Unterstützung, Verstärkung) in der Behandlung von Depressionen hat. Ich halte die Studienlage, die zu diesen Zulassungen geführt hat, für nicht gerade überwältigend. Jeder sollte sich selbst ein gut informiertes Bild darüber machen, für wie wirkstark er Quetiapin in diesen Indikationen hält. Ich halte es hier nicht für sehr wirkstark. Dasselbe gilt für die Zulassung von Aripiprazol in der Indikation als Phasenprophylaktikum.
- Und noch weniger helfen Neuroleptika bei gewünschten Verhaltensänderungen aus dem Bereich der Pädagogik. Das Behandlungsziel, jemand möge sich in irgend einer Form sozial adäquater verhalten oder sei irgendwie „nicht mehr führbar“ oder „nicht mehr haltbar“ ist immer dann, wenn diese Verhaltensänderung nicht psychotisch bedingt ist, keine Indikation für ein Neuroleptikum.
Neuroleptika bremsen die dopaminerge Neurotransmission. Dopamin aber ist unerläßlich für Antrieb, Motivation und Freude. Daher darf ein Eingriff in diesen Transmitterhaushalt nur erfolgen, wenn eben dieser Transmitterhaushalt krankheitsbedingt überaktiv ist. Und sonst nicht. Egal, wie verzweifelt der Behandler ist.
Amphetamine verschlechtern Tic-Symptomatik
Das Gille-de-la-Tourette-Syndrom ist ein eher seltenes, aber sehr beeinträchtigendes Krankheitsbild, bei dem die Betroffenen den unwiderstehlichen Drang haben, bestimmte motorische oder vokale Tics auszuführen. Bekannt ist das Krankheitsbild vor allem aus Komödien und Fernsehfilmen, in denen ein Betroffener immer wieder aggressive oder obszöne Worte ausstößt, das heißt dann Koprolalie.
Pharmakotherapeutisch wird beim Tourette-Syndrom in erster Linie Tiaprid eingesetzt, das allgemein eine gute Wirkung auf extrapyramidale Hyperkinesien hat. In zweiter Linie wird oft Haloperidol eingesetzt, ein bekanntermaßen dopaminantagonistisches Neuroleptikum.
Die meisten der Patienten mit einem Tourette-Syndrom, die ich kenne, kommen mit Tiaprid alleine ganz gut hin. Von den wenigen, die ich kenne, die zusätzlich Haldol nehmen, geben allerdings alle an, dass dieses ihnen einen zusätzlichen Nutzen bringt und die Tic-Symptomatik merkbar reduziert.
Ich selbst bin immer etwas skeptisch, wenn Psychiater bei nicht-psychotischen Symptomen ein Neuroleptikum zusätzlich zu einer anderen Therapie verordnen. Ich frage mich dann immer, ob das nun mehr Ausdruck einer gewissen therapeutischen Verzweiflung ist (Neuroleptika helfen ja bei Psychosen so durchschlagend, dann helfen sie doch bei anderen psychiatrischen Erkrankungen vielleicht auch ein bischen, oder?), oder ob es wirklich etwas bringt. Ich war mir nie ganz sicher, ob gerade das Tourette-Syndrom als extrapyramidale Störung nun ausgerechnet von Haloperidol profitiert.
Und nun hat mir vor einiger Zeit ein Patient, der unter einem ausgeprägten Tourette-Syndrom mit starken vokalen Tics leidet, berichtet, dass die Tic-Symptomatik deutlich schlechter wird, wenn er Amphetamine nimmt. Das ist pharmakologisch interessant, da Amphetamine Dopamin und Noradrenalin freisetzen.
Derselbe Patient berichtet, dass bei ihm die Gabe eines Neuroleptikums, dass unter anderem den Dopamin-Stoffwechsel kontrolliert, die Tics reduziert; unabhängig davon, ob er nun gerade Amphetamine genommen hat oder nicht.
Die Verschlechterung der motorischen und verbalen Tics unter Amphetaminen gibt einen Hinweis darauf, dass dopaminantagonistische Neuroleptika tatsächlich eine gezielte und ursächliche Therapie des Tourette-Syndroms sein können.
Depot Neuroleptika: Umrechnung der oralen Dosis in eine Depot-Dosis
Depot Neuroleptika
Depotneuroleptika können in manchen Fällen praktischer sein als oral gegebene Neuroleptika, namentlich, wenn der Patient diese Applikation bevorzugt und eine orale Medikation auf praktische Schwierigkeiten trifft. Eine Depotmedikation ist jedoch ungeeignet, wenn der Patient die Medikation an sich nicht wünscht. Depotgaben gehen, anders als die Tablettenform, regelmäßig mit der Gefahr einher, dass ein Spritzenabszess entstehen kann, sodass aus meiner Sicht diesem Nachteil der Depotform ein eindeutiger Vorteil gegenüber stehen muss.
Umrechnung Orale Dosis Neuroleptikum in Depot Dosis
Bei Einstellung auf ein atypisches Depot ist es in aller Regel sinnvoll, in den ersten 2-4 Wochen den Depotwirkstoff parallel auch oral zu geben, da es üblicherweise so lange dauert, bis ein Blutspiegel im Therapeutischen Bereich aufgebaut ist. Im Zweifel sollte man den Blutspiegel laborchemisch bestimmen.
Es stellt sich dann die Frage, welche Depotdosis zu wählen ist. Es gibt keine einfache Formel, um die oral gegebene Dosis eines Neuroleptikums in eine Depot-Dosis umzurechnen. Aber man versucht es doch immer wieder…. Ich habe hier mal eine Tabelle erstellt, die einen Anhalt gibt, welche Dosierungen oral gegeben welcher Depot-Dosis und welchem Depot Intervall in etwa entsprechen. Wie immer ohne Gewähr, es bildet meine persönliche Anwendung ab, aber keine Wahrheiten…
Der Umrechnungsfaktor ist so zu verstehen: x mg orale Dosis entsprechen x mal Umrechnungsfaktor mg Depotdosis. Dabei ergibt sich in den meisten Fällen die Depot-Dosis, die alle zwei Wochen zu geben ist, manchmal ist der Umrechnungsfaktor aber auch so berechnet, dass sich die Dosis für das das Vier-Wochen Intervall ergibt, je nach dem, welches Intervall bei diesem Depot üblich und pharmakologisch sinnvoll ist. Viele Depots können auch in längeren Intervallen gegeben werden, was die Wahrscheinlichkeit eines Spritzenabszesses entsprechend reduziert.
| Dosierung in Worten | Dosierung in Tablettenform | Faktor | Depotdosierung |
|---|---|---|---|
| Flupentixol, z.B. Fluanxol® | |||
| Niedrig | 4–0–0 mg | 5 | 20 mg alle 2 Wochen |
| Mittel | 10–0–0 mg | 5 | 50 mg alle 2 Wochen |
| Hoch | 10–10–0 mg | 5 | 100 mg alle 2 Wochen |
| ❊ | |||
| Risperidon, Risperdal Consta® | |||
| Niedrig | 0–0–2,5 mg | 10 | 25 mg alle 2 Wochen |
| Mittel | 0–0–4 mg | 10 | 37,5 mg alle 2 Wochen |
| Hoch | 0–0–5 mg | 10 | 50 mg alle 2 Wochen |
| ❊ | |||
| Paliperidon, Xeplion® | |||
| Xeplion® Einstellung auf jede Dosis immer so beginnen: Tag 1: 150 mg deltoidal, Tag 8: 100 mg deltoidal, danach: | |||
| Niedrig | 3–0–0 mg | 15 | 50 mg alle 4 Wochen |
| Mittel | 6–0–0 mg | 15 | 75 mg alle 4 Wochen |
| Hoch | 6–0–6 mg | 15 | 100 mg alle 4 Wochen |
| ❊ | |||
| Haloperidol, z.B. Haldol® | |||
| Niedrig | 2–0–2 mg | 10 | 40 mg alle 4 Wochen |
| Mittel | 4–0–4 mg | 10 | 80 mg alle 4 Wochen |
| Hoch | 6–0–6 mg | 10 | 120 mg alle 4 Wochen |
| ❊ | |||
| Fluphenazin, z.B. Lyogen® | |||
| Niedrig | 2–0–3 mg | 5 | 25 mg alle 2 Wochen |
| Mittel | 5–0–5 mg | 5 | 50 mg alle 2 Wochen |
| Hoch | 10–0–10 mg | 5 | 100 mg alle 2 Wochen |
| ❊ | |||
| Olanzapin, ZypAdhera® (W=Wochen) | |||
| Niedrig | 0–0–10 mg | 20 | 210 mg/2 W oder 405 mg/4 W für 8 W. Dann 150 mg/2 W oder 300 mg/4 W |
| Mittel | 0–0–15 mg | 20 | 300 mg/2 W für 8 W. Dann 210 mg/2 W oder 405 mg/4 W |
| Hoch | 0–0–20 mg | 20 | 300 mg alle 2 Wochen |
| Aripiprazol, Abilify Maintena® | |||
| Mittel | 10-0-0 mg | 20 | 300 mg alle 4 Wochen |
| Hoch | 20–0–0 mg | 20 | 400 mg alle 4 Wochen |
Literatur
- Praktische Psychopharmakotherapie, Laux, G.; Dietmaier, O.; 2012
- Guidelines for the Dosage of Neuroleptics. II: Changing from Daily Oral to long Acting Injectable Neuroleptics. Schulz, P.; Rey, MJ.; Dick, P.; Tissot, R. Inernational Clinical Psychopharmacology, 1989, 4, 105–114
- Fachinformation Fluanxol
- www.zypadhera.de
Copyright
Dieser Beitrag ist ein Auszug beziehungsweise eine auszugsweise Vorabveröffentlichung des Werks „Psychopharmakotherapie griffbereit“ von Dr. Jan Dreher, © Georg Thieme Verlag KG. Die ausschließlichen Nutzungsrechte liegen beim Verlag. Bitte wenden Sie sich an permissions@thieme.de, sofern Sie den Beitrag weiterverwenden möchten.
Welches Neuroleptikum gebe ich wem?
Nehmen wir an, in meine Behandlung kommt ein sonst gesunder Patient mit einer Psychose. Ich entscheide mich, dass er ein Neuroleptikum braucht. Das bespreche ich mit ihm und er stimmt dem auch zu. Nun stellt sich die Frage: Welches Neuroleptikum empfehle beziehungsweise verordne ich? Es gibt keine ganz einfache Faustformel, nach der ich für einen bestimmten Patienten ein Neuroleptikum auswähle, aber ich habe ein bestimmtes Vorgehen, dass ich in bestimmten Fällen anwende. Ich habe hier mal versucht, dies aufzuschreiben:
Welches Neuroleptikum gebe ich wem?
Konstellation 1: Der erfolgreich vorbehandelte Patient: Auf meine Frage: „Haben Sie schon einmal in einer früheren Krankheitsphase ein Neuroleptikum erhalten? Hat es gut gewirkt und haben Sie es gut vertragen?“ antwortet er zwei mal mit „Ja“, d.h. ein bestimmtes Präparat hat schon einmal gut gewirkt und wurde gut vertragen. Dann empfehle ich genau dieses Medikament wieder. Ich frage, welche Symptomatik damals bestanden hat und wie stark sie war und welche Dosis des Präparates in welcher Zeit geholfen hat. Ich mache mir ein Bild davon, wie stark die Symptomatik jetzt ist und empfehle eine passende Dosis.
Konstellation 2: Der bislang unbehandelte Patient: Wenn bislang noch nie ein Neuroleptikum verordnet wurde empfehle ich in der Regel in der ersten Stufe Risperidon. Es wirkt schnell und verläßlich. Es macht nicht müde und es macht keine Gewichtszunahme. Wenn ich selbst ein Neuroleptikum bräuchte, würde ich mich auch für Risperidon entscheiden. (Das stimmt sogar mit dem Ergebnis meiner kleinen Umfrage überein: Welches Neuroleptikum würdest Du selbst einnehmen: hier). In Dosierungen bis 4 mg pro Tag ist es meist gut verträglich und macht meist keine EPMS. In höheren Dosierungen kann es EPMS machen.
Konstellation 3: Risperdal hat nicht ausreichend geholfen oder wurde nicht vertragen. Der Pat. ist nicht adipös: In der zweiten Stufe empfehle ich in der Regel Zyprexa (nachdem ich über die Möglichkeit einer Gewichtszunahme aufgeklärt habe). Es wirkt ebenso sicher, verläßlich und zügig wie Risperidon und wird ebenfalls zumeist gut vertragen. Es kann aber tatsächlich eine deutliche Gewichtszunahme verursachen. Daher lasse ich das Gewicht bei Beginn der Behandlung mit Zyprexa messen. Treten Heißhungerattacken oder eine Gewichtszunahme von mehr als 3 Kilogramm auf, empfehle ich, das Präparat zu wechseln.
Konstellation 4: Zyprexa hat nicht ausreichend geholfen oder wurde nicht vertragen: Wenn Risperdal in Stufe eins wegen mangender Wirksamkeit und nicht wegen EPMS das Feld räumen musste, und in Stufe zwei Zyprexa nicht gut ging, dann versuche ich in der dritten Stufe Solian. Wenn Risperdal EPMS gemacht hatte, dann überspringe ich diesen Schritt.
Konstellation 5: Mit Risperdal, Zyprexa und Solian stellte sich kein Erfolg ein: In der vierten Stufe muss ich ein Neuroleptikum auswählen, dass gegebenenfalls etwas weniger wirkstark ist als Risperdal, Zyprexa und Solian, aber vielleicht besser verträglich ist. Es kommen nun Abilify, Zeldox, Seroquel (meine Einschätzung zu Seroquel findet ihr hier) und Serdolect in Betracht. Ich verordne in dieser Reihenfolge. Abilify führt häufig zu Akathisie, ich setzte es dann zumeist sofort und ohne zu warten ab. Zu Serdolect sind diese Hinweise zu beachten. Zeldox und Seroquel werden in der Regel sehr gut vertragen, hier stellt sich eher die Frage der ausreichenden Wirksamkeit.
Konstellation 6: Eine Monotherapie klappt nicht: In der fünften Stufe wähle ich eine Kombinationstherapie aus zwei Neuroleptika. Geleitet von den Nebenwirkungen der bisherigen Versuche wähle ich gut verträgliche, aber in Monotherapie nicht ausreichend wirksame Präparate aus und gebe beide in einer mittleren Dosis. Dabei unterteile ich die Neuroleptika nach ihren Nebenwirkungen in unterschiedliche Gruppen und meide die Gruppe, deren Nebenwirkung bislang am problematischsten war:
- Gruppe 1: EPMS-Gefahr: Haldol, Solian, Risperdal
- Gruppe 2: Gewichtszunahme-Gefahr: Clozapin, Zyprexa, manchmal Seroquel
- Gruppe 3: Akathisie-Gefahr: Abilify
Konstellation 7: Alle oben genannten Stufen wurden nicht gut vertragen: Ich versuche Serdolect.
Konstellation 8: Alle oben genannten Stufen haben nicht ausreichend gewirkt: Ich kläre ausführlich auf und versuche Clozapin.
Konstellation 9: Reine Rezidivprophylaxe bei asymptomatischem Patienten: Mit großer Sicherheit wirkt das Neuroleptikum, das die psychotische Episode beendet hat. Bei der Rezidivprophylaxe sind aber Nebenwirkungen noch viel weniger akzeptabel als in der Akuttherapie. Bei Nebenwirkungen wechsele ich daher noch niederschwelliger auf ein Ausweichpräparat.
Konstellation 10: Behandlung akuter kokaininduzierter psychotischer Zustände: Kokain ist stark und selektiv dopaminagonistisch. Solian ist stark und selektiv dopaminantagonistisch. Daher behandele ich akute psychotische Zustände nach Kokainkonsum mit Solian.
Konstellation 11: Delir: Ein lebensbedrohliches Delir, egal welcher Genese (Alkoholentzug-, Benzodiazepinentzug-,…) braucht eine wirkstarke und schnelle Neurolepsie. Ich gebe Haloperidol oder Risperidon.
Konstellation 12: Auswahl eines Depotpräparates: Ich mache zunächst einen Versuch mit Fluanxol, zunächst oral gegeben. Wird dies vertragen, gebe ich eine milde Dosis Fluanxol Depot, etwa 40-60 mg alle zwei Wochen. Sind bei dem Patienten unter irgendeiner Medikation EPMS aufgetreten, gebe ich Risperdal Consta oder Xeplion. Immer noch EPMS: Dann Zypadhera. (Zu Depotpräparaten siehe auch hier)
Das ist natürlich nur eine Blaupause, bei jedem einzelnen Patienten können so viele weitere Aspekte eine Rolle spielen, dass diese Blaupause nicht hilft. Aber manchmal hilft sie doch.
OK, das waren jetzt so einige Gedanken, die ich oft anwende. Wie gehst Du vor? Was machst Du anders? Bitte schreib Dein Vorgehen in die Kommentare!
P.S.: Hier der Artikel zur Auswahl eines Antidepressivums.
Copyright
Dieser Beitrag ist ein Auszug beziehungsweise eine auszugsweise Vorabveröffentlichung des Werks „Psychopharmakotherapie griffbereit“ von Dr. Jan Dreher, © Georg Thieme Verlag KG. Die ausschließlichen Nutzungsrechte liegen beim Verlag. Bitte wenden Sie sich an permissions@thieme.de, sofern Sie den Beitrag weiterverwenden möchten.
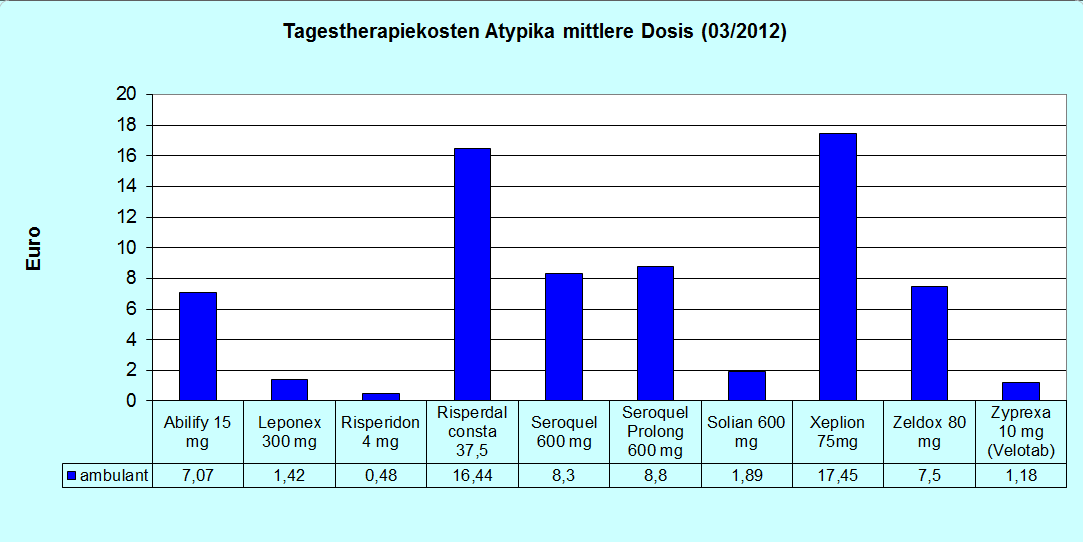
Tagestherapiekosten atypischer Neuroleptika im ambulanten Bereich
Die Tagestherapiekosten atypischer Neuroleptika unterscheiden sich sehr. Die Präparate mit noch bestehendem Patent sind teuer, geführt von den Depot-Präparaten Zypadhera (300 mg alle zwei Wochen kosten 32,50 € pro Tag), Xeplion und Risperdal consta mit etwa 22 € am Tag.
Es folgen die patentgeschützten Tablettenformulierungen Abilify, Seroquel und Zeldox mit etwa 8 € pro Tag. Das Patent von Seroquel in der unretardierten Form ist noch nicht abgelaufen, es läuft aber zum 24.03.2012 ab. Dann werden die Kosten von jetzt etwa 12 € am Tag sicher fallen.
Die Präparate, deren Patent abgelaufen ist, liegen oft unter 3 € pro Tag (Leponex, Risperdal, Solian, Zeldox, Zyprexa). Die Grafiken geben einmal den Preis für eine hochdosierte Behandlung wieder und einmal den Preis für eine mittelhoch dosierte Therapie. Die Preise im stationären Bereich liegen niedriger.
Sterbende Mythen Teil 7924: „Eine Depot Medikation erhöht die Compliance!“
Wenn ein psychiatrischer Patient, der eine neuroleptische Medikation braucht, diese immer wieder nach einer gewissen (zu kurzen) Zeit entgegen ärztlichen Rat absetzt, rufen Angehörige und semiprofessionelle Helfer in unermüdlicher Gleichförmigkeit: „Sie müssen ihn auf ein Depot einstellen. Dann ist sichergestellt, dass er es auch nimmt.“ Stimmt. Und zwar genau einmal, und dann wirkt es genau zwei (bis max. vier) Wochen. Und dann kann er es wieder nehmen, oder eben nicht. Einwurf Semiprofessionalität: „Jaaaah, aber dann kriegen Sie und wir und alle Welt das wenigstens mit! Ha!“
Stimmt auch. Und dann? Dann wissen alle, dass er seine Neurolepsie nicht mehr nimmt. Hätte man ihn auch fragen können. Aber gut, so weiß man es, weil er nicht in die Praxis kommt. Und nun? Es gibt praktisch kaum eine Möglichkeit, jemanden dazu zu zwingen, sich ein Depot spritzen zu lassen. Man kann einen Betreuungsbeschluß beantragen, in dem steht, dass die Nichtabholung des Depots zu einer Unterbringung im Krankenhaus führen soll, und dass dort dann das Depot gegeben werden soll. Habe ich schon einige Male gemacht. Und hatte dann alle zwei Wochen die Situation, mit Hilfe der Betreuungsstelle, der Feuerwehr und Zwang die Einweisung ins Krankenhaus zu organisieren. Ohne sehr triftigen Grund macht man das nicht all zu lange…
Wenn ein Patient eine Neurolepsie nicht nehmen möchte, und es keine gesetzliche Grundlage gibt, ihn zu zwingen, wie am ehesten eine Bewährungsauflage, dann kann er auch eine Depotmedikation jederzeit absetzen. OK, man sieht es frühzeitig.
Depots haben große Vorteile, wenn jemand zwar alle zwei oder vier Wochen einen Arzt aufsucht, aber zwischenzeitlich eine Tabletteneinnahme nicht hinbekäme, etwa weil er obdachlos ist, und das Depot bevorzugt, oder weil er die Medikation zwar will, aber die Tabletteneinnahmeihm zu lästig oder kompliziert ist oder er sie wirklich häufiger mal vergißt, er die Neurolepsie also will, aber unzuverläßig oder unregelmäßig einnimmt. Dann hilft das Depot. Aber nicht, wenn jemand keine Neurolepsie will. Das das Depot dann die Compliance erhöht, ist ein Mythos. Gut verträgliche Tabletten gehen dann sogar mit einer höheren Compliance einher als ein weniger gut verträgliches Depot. Das ist die Erfahrung.
Rezeptorbindungsprofile der Neuroleptika: Die Persönlichkeit der wichtigsten Neuroleptika auf einen Blick
Um das Profil eines Neuroleptikums zu lesen, reichen fürs erste folgende Daumenregeln:
- D2 Rezeptor: Typische Neuroleptika sind D2 Antagonisten, z.B. Haldol: Sichere antipsychotische Wirkung, aber bei hohen Dosierungen EPMS
- 5-HT 2A Rezeptoren: Atypische Neuroleptika sind 5-HT 2A Antagonisten: Gute Antipsychotische Wirkung, wenig EPMS
- D4 Rezeptor: Clozapin hat eine außergewöhnlich hohe Affinität zum (sehr seltenen) D4 Rezeptor; möglicherweise wirkt dies antipsychotisch, ohne viel EPMS zu verursachen.
- H1 (Histamin): Müdigkeit
- Alpha-1=Alpha-Adrenerge Rezeptoren der Untergruppe 1: Vegetative Nebenwirkungen wie Orthostase, Schwindel, etc.
OK, das ist jetzt extrem vereinfacht, aber schon mal ein Anfang. Im Falle des Aripiprazols muss man wissen, dass die Affinität zum D2 Rezeptor nicht nur antogonistische, sondern auch partiell agonistische Wirkungen hat, weswegen es deutlich weniger EPMS macht, als das Schaubild vermuten lassen könnte.
Gut, schauen wir mal, ob wir mit diesem Wissen etwas erkennen können. Bitte schau Dir jetzt das Bild noch mal genau an (auf das Bild clicken, um es zu vergrößern). Ich stelle Dir ein paar Fragen:
- Nimm Dir Risperidon. Macht es EPMS?
Antwort: Schon ein bisschen, denn es blockiert den D2 Rezeptor. In hohen Dosierungen also schon. - Olanzapin: EPMS?
Antwort: Wenig, aber möglich ist es schon, denn auch Olanzapin blockiert nicht unwesentlich den D2 Rezeptor. Und das passt auch zur klinischen Beobachtung, dass Olanzapin schnell und sicher antipsychotisch wirkt, aber ab 30 mg pro Tag oft EPMS machen kann. Bei manchen Patienten aber auch schon deutlich niedrigeren Dosierungen. - Olanzapin: Müdigkeit?
Antwort: Klar, deutliche H1 Komponente. - Quetiapin: Macht es EPMS?
Antwort: Nein, fast keine D2 Blockade. - Quetiapin: Macht es müde, macht es vegetative Nebenwirkungen?
Antwort: Ja, H1 und Alpha-1 Blockade sind ausgeprägt. - Quetiapin: Antipsychotische Wirkstärke relativ zur Sedierung:
Antwort: Vergleiche 5-HT 2A plus D2 Blockade relativ zu H1 und alpha 1 Blockade. - Ziprasidon: EPMS?
Antwort: In höherer Dosierung ja, D2 Blockade. - Ziprasidon: Müdigkeit?
Antwort: Nein, praktisch keine H1 Komponente.
Du siehst, die Vermutungen, die man aufgrund der Daumenregeln oben anstellt, wenn man das Rezeptorbindungsprofil anschaut, passen oft ganz gut zum klinischen Eindruck. Die Persönlichkeit des Medikamentes, seine Vorzüge und Nachteile, bilden sich in dieser Grafik gut ab.
Es ist sinnvoll, sich eine Grafik mit den Rezeptorbindungsprofilen der Neuroleptika, die man oft verschreibt, immer wieder anzugucken. Man lernt die Medikamente so besser kennen.
In späteren Blog-Einträgen möchte ich gerne genauer auf einzelne Medikamente eingehen und auch zu den einzelnen Rezeptoren mehr sagen. Dieser Eintrag soll aber erst einmal einen Überblick geben und erklären, wie man das Rezeptorprofil, dargestellt als Kuchendiagramm, grundsätzlich liest.