Die meisten Ärzte sagen dazu: „Nein, verzichten sie am Besten ganz auf Alkohol, wenn sie Medikamente einnehmen“. Das ist ja auch ein gut gemeinter Rat. Aber die Wahrheit ist etwas differenzierter. Wenn du wirklich wissen willst, welche Wechselwirkungen zwischen Alkohol und bestimmten Psychopharmaka typischerweise auftreten können, und welche Überlegung ich anstelle, wenn ich diese Frage beantworte, dann guck dir dieses Video an…
Psychiatrie
Morgen ist bei uns „Stromloser Tag“

Also, wir sind vorbereitet. Morgen feiern wir mit den Kindern den „stromlosen Tag“. Gut, der Kühlschrank bleibt eingeschaltet, ich will ja nicht meine geliebten tiefgefrorenen Gemüse verlieren. Alle anderen elektronischen Geräte bleiben für einen Tag ausgeschaltet und wir machen lauter umweltfreundliche Sachen. Wir haben uns sogar schon Papier Bücher beschafft. Strange…
PC096 Wie wir Erstgespräche und Aufnahmegespräche führen ist online
Liebe HörerInnen, liebe Fans, in der 96. Sendung des PsychCasts sprechen wir darüber, was wir bei Erstuntersuchung in der ambulanten Psychosomatik und der stationären Psychiatrie beachten und wie wir ungefähr vorgehen.
Außerdem geben wir das Datum des diesjährigen Hörertreffens im Rahmend des DGPPN-Kongresses bekannt, sprechen über neue Fundsachen und freuen uns, dass wir mal wieder quality-time zusammen haben.
Was die aktuelle Episode mit Tiefkühlgemüse zu tun hat, erfahrt in der Show. Viel Spaß. Sagt mal in den Kommentaren Bescheid, was Ihr davon haltet…!
Die aktuelle Folge als Video findest Du hier. Als Audio-Datei findest du die Folge hier.
Links zur Show:
- Unser Partner Blinkist mit 25%-Vorteil für Euch
- PsychCast-Freundeskreis
- PsychCast bei Twitter
- PsychCast bei Facebook
- PsychCast-Kanal bei YouTube – bitte klicke auf ABO!
Hab Mut zu mehr Therapeutischer Dynamik!
Ich hab hier mal wieder ein Video hochgeladen…:
Methadon kann die QTc-Zeit verlängern, Polamidon nicht.
Methadon kann in Dosierungen über 100 mg pro Tag recht ausgeprägte QTc-Zeit-Verlängerungen verursachen.
Methadon besteht aus zwei Stereoisomeren, dem linksdrehenden und schmerzstillenden Levomethadon und dem rechtsdrehenden, nicht schmerzstillenden Dextromethadon. Eine genauere Erklärung findet ihr hier.
Die Verlängerung der QTc-Zeit unter Methadon wird jedoch nur von Dextromethadon verursacht. Wenn ein Patient unter dem „Gemisch“ Methadon eine relevante QTc-Zeit Verlängerung entwickelt hat, hilft es, ihn auf das „reine“ Levomethadon (aka L-Polamidon) umzustellen. Dies verursacht in der Regel keine QTc-Zeit Verlängerung.
Literatur
Die Straßenpreise für illegale Drogen sinken

Nach dem, was die Polizei so berichtet, sinken gegenwärtig die Straßenpreise für Cocain, Amphetamine und Heroin; zugleich wird beobachtet, dass Cocain, MDMA und Heroin in höheren Reinheitsgraden auf dem Straßenmarkt ankommen. Das ist wichtig zu wissen, da die Konsumenten, die ja üblicherweise nicht wissen können, welchen Wirkstoffgehalt ihre Droge denn nun genau hat, leicht in die Situation einer Überdosierung kommen. Preise und Reinheitsgrade der Drogen unterscheiden sich an verschiedenen Orten und bei verschiedenen Dealern natürlich stark. Ich habe dennoch einmal versucht, hier eine Orientierung zu schaffen. Die Preise der Reinsubstanz und die typischen Wirkstoffkonzentrationen habe ich dem Europäischer Drogenbericht: Trends und Entwicklungen 2019 entnommen. Die typischen Straßenpreise pro Konsumeinheit habe ich aus mehreren verschiedenen Berichten, auch nach Aussagen von Polizei und Drogenkonsumenten, zusammengestellt.
Sind diese Angaben realistisch? Hast Du andere Beobachtungen gemacht? Hinweise bitte gerne hier in die Kommentare!
Dieser Beitrag ist ein Auszug beziehungsweise eine auszugsweise Vorabveröffentlichung des Werks „Psychopharmakotherapie griffbereit“ von Dr. Jan Dreher, © Georg Thieme Verlag KG. Die ausschließlichen Nutzungsrechte liegen beim Verlag. Bitte wenden Sie sich an permissions@thieme.de, sofern Sie den Beitrag weiterverwenden möchten.
Moderne Behandlung des Delirs: Ein how-to-Video für Praktiker
Im Delir gebe ich doch immer Haldol und Diazepam, oder? Warum das fast immer falsch ist, und wie ich es nach dem aktuellen Stand der Wissenschaft richtig machen kann, erkläre ich euch in diesem Video.
Midazolam nasal ist eine gute Option zur Sedierung im Notfall
Midazolam
- wird überwiegend in der Anästhesie und Notfallmedizin verwendet
- ist ein Benzodiazepin mit einer sehr kurzen Halbwertszeit von ca. 1,5 – 2,5 Stunden
- kann im Notfall als Nasenspray verabreicht werden
- wird im Notfall bei Erwachsenen mit 10 mg dosiert, wobei 5 mg pro Nasenloch appliziert werden
- fällt in Einheiten von mehr als 15 mg je abgeteilter Einheit unter die Betäubungsmittel
In der Anästhesie wird Midazolam gerne zur Prämedikation vor Operationen, auf Intensivstationen zur Dauersedierung oder zusammen mit Ketamin im Rahmen von Narkosen verwendet. Im Rettungsdienst wird es schon länger zur Behandlung von Krampfanfällen gegeben. Gerade hier ist eine nasale Gabe über einen Zerstäuber sehr praktisch, da es während eines Krampfanfalles schwierig ist, einen intravenösen Zugang zu legen. In den letzten Jahren hat Midazolam als nasale Gabe eine zusätzliche Nische gefunden. Auch bei einem psychiatrisch bedingten akuten Erregungszustand kann man Midazolam gut nasal applizieren. Es führt in dieser Situation zu einer zügigen Sedierung und Entaktualisierung. Die nasale Gabe ist gerade im Rahmen einer Zwangsmedikation für Behandler und Patienten sicherer als die intravenöse Gabe.
Pharmakologie
Midazolam ist ein kurzwirksames Benzodiazepin. Wenn es – wie hier beschrieben – im Rahmen der Sedierung bei akutem Erregungszustand nasal verabreicht wird, umgeht man den first-pass-Effekt. Die Wirkung tritt oft bereits nach wenigen Minuten ein.
Fallbeispiel
Der aus Vorbehandlungen gut bekannte 35 jährige Herr M. leidet seit einigen Jahren unter einer drogeninduzierten Psychose. Unter Drogenintoxikationen kam es in der Vergangenheit immer wieder zu ausgeprägten Erregungszuständen, teilweise mit fremdaggressivem Verhalten. Aktuell wird Herr M. von der Polizei auf der Rechtsgrundlage eines PsychKG´s zur Klinik gebracht. Er ist mit Handschellen fixiert, dennoch im Rahmen eines akuten Erregungszustandes nur schwer zu halten. In gesunden Zeiten hat der Patient eine Patientenverfügung erstellt, in der er dem Einsatz von Midazolam Nasenspray zu Sedierung in solchen Situationen zugestimmt hat. Darauf angesprochen stimmt er auch jetzt der Gabe von Midazolam Nasenspray zu. Der Dienstarzt nimmt sich eine Ampulle Midazolam mit 15 mg Midazolam in 3 ml Injektionslösung und zieht sie unverdünnt in eine 5 ml Spritze auf, so dass in der Spritze nun 15 mg Midazolam sind. An der Spitze der Spritze bringt er einen Mikrozerstäuber zur Vernebelung des Wirkstoffes mit darunterliegendem Schaumstoffkonus (Mucosal Atomization Device, MAD) an. Er gibt in jedes Nasenloch des Patienten einen Milliliter, entsprechend 5 mg pro Seite, dabei hält er das andere Nasenloch zu und bittet den Patienten, einzuatmen. Danach verbleibt ein Milliliter, entsprechend 5 mg Midazolam in der Spritze. Diese Dosis könnte bei unzureichender Wirkung nach einigen Minuten nachgegeben werden. Nach 5 Minuten beruhigt sich der Patient sichtlich und eine weitere nasale Medikamentengabe ist nicht erforderlich. Nach einem geordneten Aufnahmegespräch nimmt der Patient eine weitere Medikation oral ein, hierunter auch Lorazepam, das zu wirken beginnt, bevor der Effekt des recht kurzwirksamen Midazolams ganz abgeklungen ist.
In oben beschriebenen Fall ist die Rechtsgrundlage der Verabreichung die Freiwilligkeit. Je nach Bundesland gibt es sehr unterschiedliche Rechtsgrundlagen für Zwangsmedikationen. Ist eine Rechtsgrundlage für eine Zwangsmedikation vorhanden und ist die Indikation gegeben, ist die Gabe von Midazolam nasal eine gut handhabbare, sichere, zügig wirksame und effektive Behandlung.
Dosierung
- Erwachsene: 10 mg Midazolam nasal, auf beide Nasenlöcher verteilen.
- Maximale Menge 1–2 ml pro Nasenloch pro Gabe. Bei größeren Mengen fraktionierte Gabe.
- Bei unzureichender Wirkung kann nach einigen Minuten eine weitere Gabe Midazolam in geeigneter Dosis erfolgen.
Nebenwirkungen
Eine schnelle Sedierung mit Midazolam kann im Einzelfall auch zu einer Übersedierung, schlimmstenfalls mit einem reduzierten Atemantrieb einhergehen. In diesem Fall ist die Gabe des Benzodiazepinantagonisten Flumazenil (z.B. Anexate®) möglich. Nach der Gabe von Midazolam nasal kann es für einige Minuten zu einer lokalen Reizung der Nasenschleimhaut kommen. Die Patienten berichten dann ein Brennen in der Nase. Dagegen ist Lidocain-Spray wirksam.
Mein persönliches Fazit
Die nasale Gabe von Midazolam ist selbst in unruhigen Situationen einfach. Es besteht sowohl für den Patienten als auch für die Behandler ein deutlich niedrigeres Verletzungsrisko im Vergleich zu einer i.v. Medikation mit einer scharfen Nadel. Da der first-pass-Effekt umgangen wird ist die Bioverfügbarkeit gut und es kommt zu einem schnellen Wirkungseintritt, oft nach etwa 5 Minuten. Ich habe Midazolam inzwischen in mehreren psychiatrischen Notfällen mit Erfolg eingesetzt und empfehle Behandlungsteams im Rettungsdienst und in psychiatrischen Kliniken, mit dieser Behandlungsoption Erfahrungen zu sammeln.
Habt ihr Erfahrung mit Midazolam nasal im Notfall? Schreibt sie gerne hier in die Kommentare!
Literatur
Wanka, Medikamente im Rettungsdienst (ISBN 978–3–13–240087–0), © 2016 Georg Thieme Verlag KG
Copyright
Dieser Beitrag ist ein Auszug beziehungsweise eine auszugsweise Vorabveröffentlichung des Werks „Psychopharmakotherapie griffbereit“ von Dr. Jan Dreher, © Georg Thieme Verlag KG. Die ausschließlichen Nutzungsrechte liegen beim Verlag. Bitte wenden Sie sich an permissions@thieme.de, sofern Sie den Beitrag weiterverwenden möchten.
Es sind noch Plätze frei

Nächste Mittwoch, den 18.September, halte ich um 16:00 einen Vortrag zum Thema „Was gibt es Neues in der Schizophrenietherapie?“ Es wird ein Erfahrungsaustausch mit Klinikärzten und Niedergelassenen. Die Veranstaltung findet statt in den Veranstaltungsräumen des Vereinsheim tv1848, Bökelstraße 63 in 41063 Mönchengladbach. Die Veranstaltung wird unterstützt von Recordati.
Es sind noch Plätze frei. Anmeldungen gerne per Email an diese Emailadresse.
Können Computerspiele ein Skill gegen Gedankenkreisen sein?
Ist die PlayStation ein guter Skill gegen Gedankenkreisen, Zwangsgedanken oder auch Dissoziationen?
Vielen Patienten helfen Handyspiele, eine Runde Zelda auf der Switch oder ein gutes Playstation Spiel, sich wieder zu erden und zurück in die Realität zu kommen. Warum also die PlayStation nicht in das Arsenal der Skill neben Sport, Eiswürfeln und Hörbüchern einreihen?
Das Video findet ihr hier.
Welches Antidepressivum gebe ich wem? Jetzt auch als Video verfügbar
Der Post „Welches Antidepressivum gebe ich wem?“ wurde hier auf dem Blog ja ausführlich diskutiert und ich bedanke mich noch einmal sehr herzlich für die Rückmeldung. Ich habe die Ergebnisse auch als Video aufgezeichnet. Welche Form mögt ihr lieber? Welche Themen mögt ihr lieber im Blog, was eignet sich gut als Video und wann ist beides sinnvoll? Schreibt eure Vorlieben mal hier in die Kommentare!
PC094 Psychose Hörerfragen ist als Video und als Audio online!
In dieser Episode beantworten wir Eure Fragen zu den Themen Psychose, schizoaffektive Störung und co. Dabei erzählen wir viel über unser Vorgehen in der Behandlung dieser Erkrankungen.
Ihr könnt diese Episode entweder auf dem PsychCast YouTube Kanal sehen, und zwar hier, oder als PsychCast Audio-Podcast, und zwar hier.
Ergänzungen zu meinem Beitrag von gestern
Ich habe gestern eine aktualisierte Version meines Post „Welches Antidepressivum gebe ich wem?“ veröffentlicht.
Vielen Dank für die Rückfragen und Anmerkungen. Ich habe tatsächlich zwei Aspekte nicht berücksichtigt, und diese beiden nun in der aktualisierten Version an gleicher Stelle ergänzt. Ich habe diese beiden Absätze hinzugefügt:
Leichte erlebnisreaktive Depressionen
Bei leichten erlebnisreaktiven depressiven Verstimmungen gebe ich keine Medikamente. Auch nicht Valdoxan, Tianeptin oder Quetiapin zur Nacht. Die Nachteile überwiegen die Vorteile. Hier wiegt insbesondere der Nachteil schwer, dass der Patient denkt, eine Verbesserung seiner Lage werde von der Medikation kommen. Dies kann seine Motivation lähmen, selbst etwas an seiner Lage zu ändern. Stattdessen fokussiere ich auf Life-Coaching, Psychotherapie und empfehle Sport.
SSRI / SNRI werden nicht vertragen, es besteht aber eine Indikation für Antidepressiva
Es gibt Patienten, die nicht in die Kategorie „Leichte erlebnisreaktive Depression“ gehören, die von einer antidepressiven Medikation profitieren würden, die aber SSRI und SNRI in der Vergangenheit nicht vertragen haben oder diese Medikamentengruppe ablehnen. In dieser Situation sind Behandlungsversuche mit Agomelatin oder Tianeptin aufgrund der besseren Verträglichkeit gerechtfertigt, wenngleich meiner Erfahrung nach die Wirkstärke dieser beiden Substanzen niedriger sein kann als die der SSRI. In der Metaanalyse von Cipriani et al. schneidet Agomelatin aber gut ab.
Ich bin für weiteres Feedback wie immer dankbar, schreibt mir einfach hier etwas in die Kommentare!
Welches Antidepressivum gebe ich wem? Mein Update 2019!
Citalopram, Escitalopram, Venlafaxin, Duloxetin, Milnacipran. Wem empfehle ich denn nun wann welches Antidepressivum? Ich hatte 2012 schon einmal meinen Algorithmus hier veröffentlicht. Inzwischen hat sich einiges getan. Insbesondere ist Escitalopram nun meine erste Wahl vor Citalopram, und mit Milnacipran ist eine weitere Option hinzugekommen.
Ich habe den Inhalt dieses Posts auch als Video aufgenommen, das findet ihr hier.
Hier findet ihr meinen neuen Algorithmus:
Wenn ich mich entschieden habe, eine antidepressive Therapie durchzuführen, muss ich mich entscheiden, ob und wenn ja welchen Wirkstoff ich auswähle. Es gibt einige unterscheidbare Konstellationen, aber natürlich keine Patentlösungen. Dieser Abschnitt beschreibt, wie ich in bestimmten wiederkehrenden Situationen oft vorgehe. Der hier beschriebene Weg ist nicht der einzig richtige. Es ist lediglich eine vereinfachte Darstellung meines typischen Vorgehens.
Leichte erlebnisreaktive Depressionen
Bei leichten erlebnisreaktiven depressiven Verstimmungen gebe ich keine Medikamente. Auch nicht Valdoxan, Tianeptin oder Quetiapin zur Nacht. Die Nachteile überwiegen die Vorteile. Hier wiegt insbesondere der Nachteil schwer, dass der Patient denkt, eine Verbesserung seiner Lage werde von der Medikation kommen. Dies kann seine Motivation lähmen, selbst etwas an seiner Lage zu ändern. Stattdessen fokussiere ich auf Life-Coaching, Psychotherapie und empfehle Sport.
Der erfolgreich vorbehandelte Patient
Hat ein Patient schon mal ein bestimmtes Antidepressivum erhalten und hat es bei guter Verträglichkeit überzeugend gewirkt, dann empfehle ich das gleiche Medikament in der gleichen Dosis wieder.
Depressive Episode mit normaler Antriebslage
In aller Regel ist meine erste Empfehlung für die Behandlung einer depressiven Episode Escitalopram. Es ist wirkstark und gut verträglich, hat kaum Wechselwirkungen und bis auf die mögliche QTc-Zeit-Verlängerung kaum relevante Nachteile. Insbesondere macht es keine Müdigkeit, keine Gewichtszunahme und nur sehr selten Unruhe, so dass ich es auch langfristig geben kann.
Stark verminderter Antrieb bei depressiver Episode
Auch bei reduziertem Antrieb im Rahmen einer depressiven Episode erwäge ich zunächst eine Behandlung mit Escitalopram. Ist der Antrieb aber sehr stark reduziert oder zeigt sich nach zwei Wochen Therapie mit Escitalopram keine Besserung des Antriebs, dann wechsele ich auf ein SNRI. Je stärker die noradrenerge Komponente ist, desto stärker antriebssteigernd ist das Medikament. Am mildesten noradrenerg ist Venlafaxin, dann kommt Duloxetin, und am stärksten noradrenerg und somit am stärksten antriebssteigernd ist Milnacipran.
Stark erhöhter Antrieb bei depressiver Episode
Besteht ein stark erhöhter Antrieb wie bei einer agitierten Depression, empfehle ich morgens Escitalopram und abends zusätzlich vorübergehend Mirtazapin 7,5 – 30 mg. Mirtazapin sediert und hilft gut und schnell gegen Schlafstörungen und Agitation. Dauerhaft ist es aber aufgrund der Sedierung und möglichen Gewichtszunahme oft ungünstig. Wenn der Patient unter der Kombinationsbehandlung eine Besserung erfährt, kann ich Mirtazapin schrittweise absetzen und die Erhaltungstherapie mit dem besser verträglichen Escitalopram fortsetzen.
SSRI / SNRI werden nicht vertragen, es besteht aber eine Indikation für Antidepressiva
Es gibt Patienten, die nicht in die Kategorie „Leichte erlebnisreaktive Depression“ gehören, die von einer antidepressiven Medikation profitieren würden, die aber SSRI und SNRI in der Vergangenheit nicht vertragen haben oder diese Medikamentengruppe ablehnen. In dieser Situation sind Behandlungsversuche mit Agomelatin oder Tianeptin aufgrund der besseren Verträglichkeit gerechtfertigt, wenngleich meiner Erfahrung nach die Wirkstärke dieser beiden Substanzen niedriger sein kann als die der SSRI. In der Metaanalyse von Cipriani et al. schneidet Agomelatin aber gut ab.
Kardiologisch vorerkrankter Patient oder Patient mit verlängerter QTc-Zeit
Ist ein Patient kardiologisch vorerkrankt, hat er eine verlängerte QTc-Zeit oder nimmt er ein oder mehrere andere Medikamente, die die QTc-Zeit verlängern, dann empfehle ich Sertralin, da dies die QTc-Zeit nicht verlängert.
Augmentation bei nicht ausreichender Wirkung der Depressionsbehandlung
Wenn trotz ausreichend langer Behandlung mit zumindest zwei geeigneten Substanzen unter Blutspiegelkontrollen die depressive Symptomatik nicht ausreichend rückläufig ist, erwäge ich eine Augmentation mit Lithium. Hier habe ich häufig deutliche Verbesserungen beobachten können.
Generalisierte Angststörung und Zwangserkrankung
- Bei milderen Fällen beginne ich mit Escitalopram in der höchsten zugelassenen Dosis.
- In schwereren Fällen beginne ich direkt mit einem SNRI, weil diese Medikamentengruppe hier erfahrungsgemäß stärker wirkt. In der Regel beginne ich aufgrund der guten Verträglichkeit mit Duloxetin. Reicht die Wirksamkeit von Duloxetin nicht aus, wechsele ich zuerst auf Milnacipran und danach auf Venlafaxin. Wird Duloxetin aufgrund von Unruhe nicht vertragen, mache ich einen Behandlungsversuch mit Escitalopram.
- Im Falle einer schweren Zwangserkrankung empfehle ich in der Regel zusätzlich zum SNRI in der höchsten zugelassenen Dosis noch 75 mg Clomipramin zur Nacht.
Somatoforme Störung und chronifizierte Schmerzstörung
Hier empfehle ich in der Regel im ersten Schritt ein SNRI wie Duloxetin oder Milnacipran. Bei chronifizierten Schmerzen empfehle ich in der Regel zusätzlich zum SNRI noch 50 mg Amitriptylin zur Nacht.
Wahnhafte Depression: EKT
Therapie der ersten Wahl bei einer wahnhaften Depression ist die EKT. Wenn diese abgelehnt wird oder aus anderen Gründen nicht durchführbar ist, gebe ich Escitalopram in Kombination mit einem Antipsychotikum, oft Risperidon oder Olanzapin.
Behandlung von begleitender Angst
Bei Patienten mit großer Angst und keiner Abhängigkeit in der Vorgeschichte erwäge ich, vorübergehend ein Benzodiazepin zu ergänzen.
Suizidalität
Bei Suizidalität erwäge ich, ein Benzodiazepin zu ergänzen. Bei akuter Suizidalität kann es sinnvoll sein, das Benzodiazepin für einige Tage in einer hohen Dosis zu geben.
Ich würdige den normalen Zeitverlauf der Besserung
- Etwa zwei Wochen nach Beginn einer antidepressiven Medikation kommt oft eine Antriebssteigerung, nach etwa vier Wochen kommt oft die Stimmungsverbesserung.
- Angststörungen verbessern sich oft etwa nach vier bis sechs Wochen
- Zwangsstörungen verbessern sich oft nach sechs bis zwölf Wochen.
Wie wählt ihr das passende Medikament aus? Schreibt mir euer Vorgehen hier in die Kommentare!
Copyright
Dieser Beitrag ist ein Auszug beziehungsweise eine auszugsweise Vorabveröffentlichung des Werks „Psychopharmakotherapie griffbereit“ von Dr. Jan Dreher, © Georg Thieme Verlag KG. Die ausschließlichen Nutzungsrechte liegen beim Verlag. Bitte wenden Sie sich an permissions@thieme.de, sofern Sie den Beitrag weiterverwenden möchten.
PSSD: Können von SSRI verursachte sexuelle Funktionsstörungen nach dem Absetzen bestehen bleiben?
Man hört in letzter Zeit zunehmend von möglichen sexuellen Funktionsstörungen, die von SSRI verursacht werden und die auch lange Zeit nach dem Absetzen der SSRI noch bestehen bleiben. Diese nennt man PSSD (Post-SSRI Sexual Dysfunction).
Sexuelle Funktionsstörungen, insbesondere ein verzögerter Orgasmus, sind während der Einnahme von SSRI nicht selten und diese Nebenwirkung ist auch gut bekannt. Die Frage ist nun, ob diese Nebenwirkung auch nach dem Absetzen des Medikamentes fortbestehen kann.
Was könnte die neurobiochemische Ursache der PSSD sein?
Es gibt schon lange Hinweise darauf, dass SSRI die Empfindlichkeit des Penis und der Klitoris für sexuelle Reize reduzieren können. Dies könnte möglicherweise eine Erklärung für die nicht selten berichtete Nebenwirkung eines verzögerten Orgasmus unter SSRI sein. In der Behandlung des Vorzeitigen Samenergusses wird tatsächlich das SSRI Dapoxetin erfolgreich eingesetzt. Es gibt Hinweise darauf, dass einige Patienten auch nach Absetzen der Antidepressiva über längere Zeit sexuelle Funktionsstörungen erleben, insbesondere scheint es Patienten zu geben, die eine nach dem Absetzen des Medikamentes länger bestehende reduzierte sexuelle Erregbarkeit, reduzierte Empfindlichkeit des Penis / der Klitoris oder eine gestörte Orgasmusfähigkeit berichten.
Besteht diese Symptomatik nach Absetzen der SSRI über längere Zeit fort, heißt das PSSD (Post-SSRI Sexual Dysfunction).
Es ist noch unklar, wie häufig PSSD tatsächlich ist, aber in der öffentlichen Diskussion ist das Thema bereits angekommen und auch die Absetzerscheinungen wurden in der Fachwelt zuerst unterschätzt. Es ist also sinnvoll, diese mögliche Nebenwirkung aufmerksam im Auge zu behalten. Habt Ihr selbst oder über eure Patienten konkrete Erfahrungen mit PSSD? Schreibt darüber gerne in den Kommentaren!
Copyright
Dieser Beitrag ist ein Auszug beziehungsweise eine auszugsweise Vorabveröffentlichung des Werks „Psychopharmakotherapie griffbereit“ von Dr. Jan Dreher, © Georg Thieme Verlag KG. Die ausschließlichen Nutzungsrechte liegen beim Verlag. Bitte wenden Sie sich an permissions@thieme.de, sofern Sie den Beitrag weiterverwenden möchten.
10 mg Escitalopram entsprechen 40 mg Citalopram !?!
Auf dem immer extrem lesenswerten Update-Blog zum Kompendium der Psychiatrischen Pharmakotherapie wurde heute von Francesca Regen aus Berlin dieser Artikel veröffentlicht, in dem erklärt wird, warum 10 mg Escitalopram nicht, wie viele denken und wie es auch weitverbreitet üblich ist, 20 mg Citalopram entsprechend, sondern dass eher eine Dosis von 40 mg Citalopram äquivalent zu 10 mg Escitalopram sind.
Zur Erklärung ist noch einmal anzuführen, dass Citalopram ein Mischung aus zwei chiralen Substanzen ist, dem linksorientierten S-Citalopram und dem rechts orientierten R-Citalopram. Das bedeutet, dass in 20 mg Citalopram 10 mg S-Citalopram oder Escitalopram sind und 10 mg R-Citalopram, das bislang für einfach wirkungslos gehalten wurde. Dieses interagiert aber offenbar sowohl pharmakokinetisch als auch pharmakodynamisch mit dem Escitalopram, so dass die klinische Vergleichsdosis zu 10 mg Escitalopram 40 mg Citalopram sei. Lest den Artikel bitte hier im Original, dort wird es gut erklärt.
Der Umrechnungsfaktor von 1 zu 4 ist für mich neu, ich war bislang immer von 1 zu 2 ausgegangen. Ich habe beispielsweise hier eine Tabelle erstellt und auch Quellenangaben gemacht, die eher zu einem Umrechnungsfaktor in der Größenordnung von 1 zu 2,2 kommen, die ich der Einfachheit halber auf 1:2 gekürzt habe.
Nun interessiert mich, wie welche Erfahrung ihr mit den beiden Substanzen gemacht habt? Welchen Umrechnungsfaktor verwendet ihr für euch? Entspricht ein Faktor von 1:4 den klinischen Erfahrungen?
Wer dazu Beobachtungen gemacht hat, schreibt sie bitte hier in die Kommentare!
Wie läuft die Facharztprüfung Psychiatrie und Psychotherapie ab?
Unser PsychCast YouTube Kanal füllt sich weiter! In diesem Video erkläre ich, wie die Rahmenbedingungen und der Ablauf der Facharztprüfung Psychiatrie und Psychotherapie in NRW sind und mache euch so schon mal etwas mit der Situation vertraut. Dieses Video ist also insbesondere für Ärzt:innen in Weiterbildung zum Facharzt für Psychiatrie und Psychotherapie interessant, die sich auf die Facharztweiterbildung vorbereiten. Alex und ich werden in unserer neuen Playlist „Ärzte / Ärztinnen in Weiterbildung“ weitere Videos in dieser Reihe posten.
Viel Spaß beim ansehen, bitte abonniert bei der Gelegenheit gleich mal den Kanal und viel Erfolg bei der Facharztprüfung!
Antidepressiva Äquivalenzdosierungen

Wenn man von einem Antidepressivum zu einem anderen wechselt, will man ja wissen, welche Dosis des neuen Medikamentes äquivalent zur Dosis des vorigen Medikamentes ist. Natürlich gibt es da so ein Bauchgefühl, was ungefähr gleichstark ist, aber erfreulicherweise gibt es auch vernünftig zusammengestellte Äquivalenzdosierungen.
Das Paper „Dose equivalents of antidepressants: Evidence-based recommendations from randomized controlled trials“1 kann hier kostenlos im Volltext heruntergeladen werden. Eine Forschergruppe, in der unter anderem Stefan Leucht aus München mitwirkte, wertete 83 Studien mit insgesamt 14131 Patienten aus, in denen verschiedene Antidepressiva in flexibler Dosis gegen Fluoxetin oder Paroxetin verglichen wurden. Die tatsächlich gegebenen mittleren Dosierungen der verschiedenen Substanzen wurden dann zu 40 mg Fluoxetin ins Verhältnis gesetzt.
In der Zusammenfassung heißt es:
„In the primary analysis, fluoxetine 40 mg/day was equivalent to paroxetine dosage of 34.0 mg/day, agomelatine 53.2 mg/day, amitriptyline, 122.3 mg/day, bupropion 348.5 mg/day, clomipramine 116.1 mg/day, desipramine 196.3 mg/day, dothiepin 154.8 mg/ day, doxepin 140.1 mg/day, escitalopram 18.0 mg/day, fluvoxamine 143.3 mg/day, imipramine 137.2 mg/ day, lofepramine 250.2 mg/day, maprotiline 118.0 mg/day, mianserin, 101.1 mg/day, mirtazapine 50.9 mg/ day, moclobemide 575.2 mg/day, nefazodone 535.2 mg/day, nortriptyline 100.9 mg/day, reboxetine 11.5 mg/day, sertraline 98.5 mg/day, trazodone 401.4 mg/day, and venlafaxine 149.4 mg/day.“
Nun hat dieser Vergleich der Wirkstärke insgesamt natürlich so seine Limitationen. Eigentlich kann man ein SSRI nicht mit einem SNRI vergleichen, weil dessen noradrenerge Wirkung bei einem SSRI gar nicht vorhanden ist. Auch bestimmte Nebenwirkungen wie Sedierung, Gewichtszunahme, Müdigkeit und andere kommen bei einem Medikament vor, beim anderen aber nicht. Das schränkt die Aussage einer solchen Vergleichstabelle natürlich ein. Aber die Tabelle soll auch nicht so tun, als könne man jedes Antidepressivum einfach in ein anderes umrechnen. Sie soll nur einen Hinweis geben, bei welcher ungefähren Dosierung ähnliche Wirkstärken zu erwarten sind.
In der oben genannten Veröffentlichung kommen Duloxetin, Milnacipran und Trimipramin leider nicht vor. Für meine eigene Aufstellung habe ich selbst für diese drei Substanzen jeweils die zulässige Tageshöchstdosis mit 40 mg Citalopram gleichgesetzt, wohlwissend, dass diese Dosierungen nicht gleich stark sein müssen. Dann habe ich die Dosierungen auf solche Dosierungen gerundet, die man mit den verfügbaren Medikamenten auch tatsächlich geben kann. Dabei habe ich manchmal die errechnete Dosis um ein paar Prozent nach oben oder unten angepaßt, um real verfügbare Tablettendosierungen zu erreichen. Bei Escitalopram habe ich der Einfachheit halber 40 mg Citalopram mit 20 mg Escitalopram gleich gesetzt. Der Studie nach wären hier 18 mg einzusetzen, aber das macht weder pharmakologisch Sinn, noch ist diese kleine Abweichung klinisch relevant.
Dann habe ich alle Werte auf Citalopram umgerechnet und nur die Medikamente aufgeführt, die ich in meinem Buch behandele. Daraus ergibt sich folgende Tabelle der Äquivalenzdosierungen:
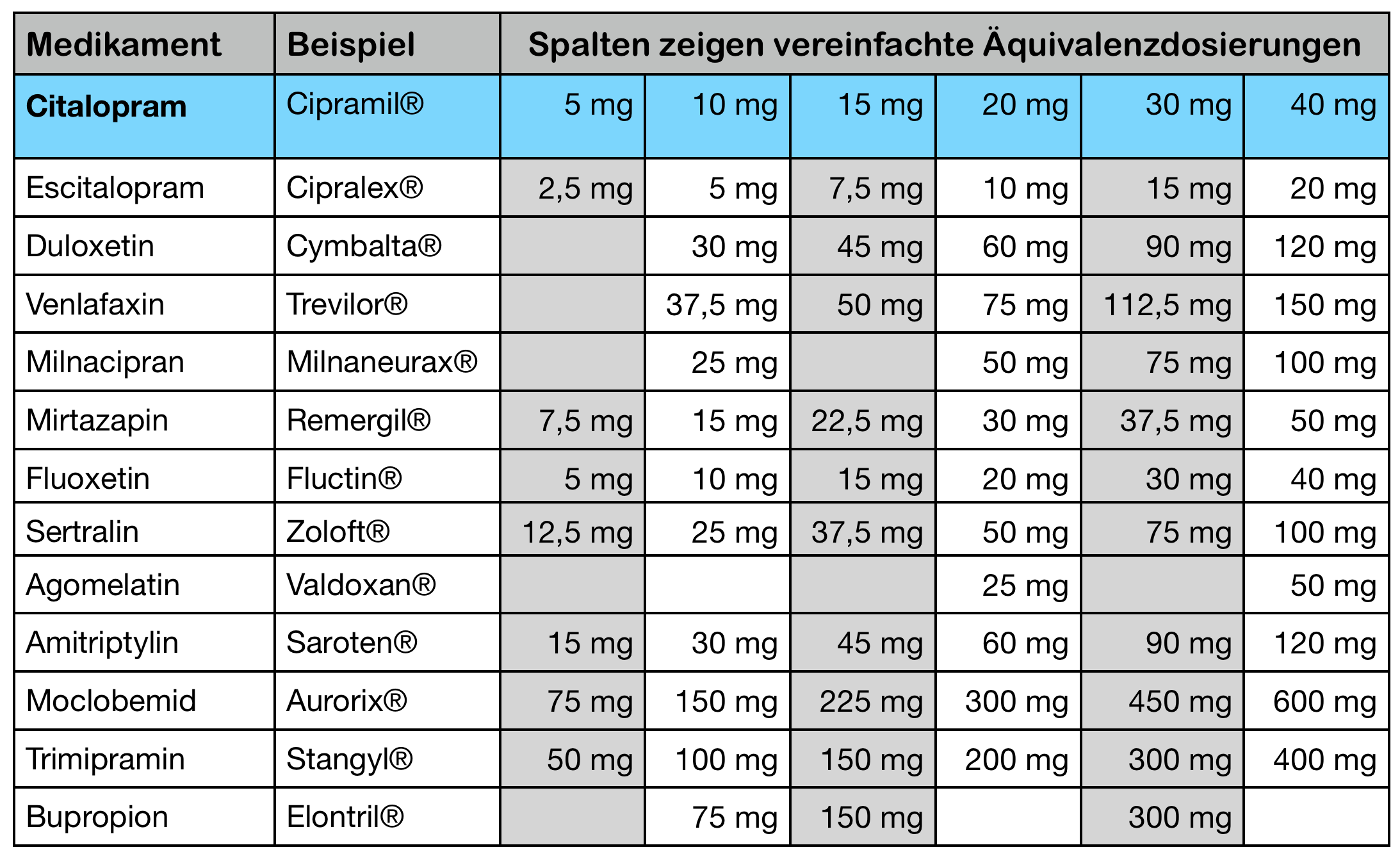
Die resultierenden Dosierungen finde ich klinisch plausibel. Sie bilden zwar nicht das genaue und von Substanz zu Substanz unterschiedliche Wirkspektrum ab, als Anhalt für vergleichbare Dosierungen vergleichbarer Wirkstärken finde ich sie aber gut verwendbar.
Was haltet ihr von dieser Überlegung? Sind die Werte plausibel? Entsprechen sie eurer klinischen Praxis? Macht eine solche Tabelle Sinn? Oder sind die Vereinfachungen, die ihr zugrunde liegen, zu groß?
Copyright
Dieser Beitrag ist ein Auszug beziehungsweise eine auszugsweise Vorabveröffentlichung des Werks „Psychopharmakotherapie griffbereit“ von Dr. Jan Dreher, © Georg Thieme Verlag KG. Die ausschließlichen Nutzungsrechte liegen beim Verlag. Bitte wenden Sie sich an permissions@thieme.de, sofern Sie den Beitrag weiterverwenden möchten.
- Hayasaka Y, Purgato M, Magni LR, Ogawa Y, Takeshima N, Cipriani A, et al. Dose equivalents of antidepressants_ Evidence-based recommendations from randomized controlled trials. Journal of Affective Disorders. Elsevier; 2015 Jul 15;180(C):179–84. ↩︎
Gelungene Online-Vorstellung psychiatrischer Kliniken: like-psychiatrie.de
Die LVR Kliniken, die Vitos Kliniken und die kbo-Kliniken haben einen Online-Kongress veranstaltet, in dessen Rahmen sich die psychiatrischen Kliniken dieser drei Träger vorgestellt haben. Der Kongress selbst ist schon vorbei, aber die Vorträge sind noch bis zum 7.7.19 abrufbar. Auf der Seite like-psychiatrie.de muss man sich zwar kurz (wenn gewünscht anonym) registrieren, aber dann kann man sich alles in Ruhe ansehen: Die Fachvorträge, die Klinikpräsentationen und das Konzept. Ich weiß, dass viele Kliniken im Rahmen des Personalrecruitings nachdenken, wie man so etwas machen könnte. Meiner Meinung nach findest Du hier ein Beispiel, wie der Gedanke der Online-Präsentation der Arbeitsbereiche, der Kliniken und einfach auch der Arbeit in der Psychiatrie wirklich sehr gut gelungen ist.
Wenn Du daran Interesse hast, registrier dich kurz und sieht sich mal um!

Das Delir
Zu diesem Thema habe ich auch ein Video bei YouTube gepostet, das findet ihr hier:
Man braucht ja immer mal einen Lehrbuchtext zum Delir. Ich habe hier einen Vorschlag erstellt. Dieser Vorschlag steht mit Blick auf die mögliche zukünftige Verwertung mal nicht unter creative commons, sondern das Copyright bleibt bei mir. Wer Lust und Zeit hat, mag ihn lesen und mir Hinweise geben, wie ich ihn noch weiter verbessern könnte. Oder sagen, dass er schon ganz gut ist… 🙂
(tl;dr: too long, didn´t read): Delir
– Das Delir ist eine reversible, typischerweise fluktuierende organisch bedingte Störung der Orientierung, des Gedächtnisses und der Aufmerksamkeit. Oft sind der Schlaf-Wach-Rhythmus gestört, es können Agitation und psychotische Symptome bestehen.– Therapeutisch müssen immer die Ursachen des Delirs behandelt werden. Darüber hinaus sollen Basismaßnahmen durchgeführt werden, wie ausreichende Flüssigkeitssubstitution, Schmerzbehandlung, Absetzen anticholinerger Medikamente, Schutz vor störenden Reizen, gute Orientierung schaffen, eigenes Hörgerät und eigene Brille zur Verfügung stellen und ähnliches.
– Benzodiazepine dann und nur dann geben, wenn Agitation besteht.
– Antipsychotika dann und nur dann geben, wenn psychotische Symptome / Halluzinationen vorliegen.
– Im Alkoholentzugsdelir sind Clomethiazol oder Benzodiazepine sowie Antipsychotika indiziert.
Psychiater haben immer wieder mit der Behandlung von Delirien zu tun. Ob als Komplikation einer Alkoholentzugsbehandlung, in der Gerontopsychiatrie bei einer einfachen Exsikkose, auf der Intensivstation als postoperatives Delir oder bei einem Übermaß an anticholinerger Medikation: Delirien zu erkennen und zu behandeln gehört zu den grundlegenden Aufgaben des Psychiaters.
Der Begriff Delir stammt vom Lateinischen „De lira ire“. „De“ heißt „aus“; „lira“ bedeutet „Gleis, Spur“ und „ire“ heißt „gehen“. Übersetzt heißt es also „aus dem Gleis gehen“ oder „aus der Spur geraten“.
Das Delir beginnt meist plötzlich aufgrund einer körperlichen Störung der Gehirnfunktion. Es zeigt typischerweise einen fluktuierenden Verlauf und ist grundsätzlich reversibel. Klinisch imponieren Desorientierung, Verkennung der Umgebung, Störungen von Gedächtnis und Aufmerksamkeit und in manchen Fällen Halluzinationen. Psychomotorisch zeigen sich Auffälligkeiten, die vom Stupor über nestelnde, ungerichtete Bewegungen hin bis zu starker Agitation reichen können. Der Schlaf ist oft im Sinne einer Schlaf-Wach-Rhythmus-Umkehr mit nächtlicher Unruhe gestört.
In der ICD-10 wird das Delir so charakterisiert:
- Störung des Bewusstseins und der Aufmerksamkeit
- Wahrnehmungsstörung (Gedächtnis, Orientierung)
- Psychomotorische Störungen
- Schlafstörungen
- Akuter Beginn und fluktuierender Verlauf
- Nachweis einer organischen Grundlage
Auf Intensivstationen sind delirante Zustände mit ca. 30-80% aller dort behandelten Patienten sehr häufig. Insbesondere postoperativ kommt es bei vielen Patienten zu Verwirrtheitszuständen.
Die früher oft verwendete Bezeichnung “Durchgangssyndrom” für postoperative Delirien verharmlost die Symptomatik allerdings und ist in dieser Hinsicht irreführend. Tatsächlich verlängern Delirien die Krankenhausbehandlungsdauer, gehen in bis zu einem Viertel der Fälle mit bleibenden kognitiven Funktionsstörungen einher und führen zu einer erhöhten Sterblichkeit.
Prävention
Es gibt gut etablierte und einfache Maßnahmen, um die Wahrscheinlichkeit des Auftretens eines Delirs zu reduzieren. Dazu gehören unter anderem:
- Orientierungshilfen wie Uhr und Kalender
- Eigenes Hörgerät, eigene Brille
- Angemessene Schmerzbehandlung
- Vermeidung unnötiger Stationswechsel
- Feste und gleichbleibende Ansprechpartner
- Frühe Mobilisierung
- Schutz vor vermeidbarem Lärm, auch durch medizinische Geräte
- Nachts möglichst dunkles Patientenzimmer
- Schlafverbesserung
- Vermeidung unnötiger Polypharmazie
- Vermeidung unnötiger anticholinerger Medikamente
Medikamentöse Prophylaxe
In den bisherigen Studien zeigte sich, dass zumindest Antipsychotika keine prophylaktische Wirksamkeit gegen die Entwicklung eines Delirs haben. Neben den oben genannten Basismaßnahmen gibt es somit aktuell keine wirksame medikamentöse Delirprophylaxe.
Diagnostik
Die Diagnostik vor allem des hypoaktiven Delirs gelingt sicherer mit etablierten Testverfahren, wie dem kostenlos in deutscher Sprache erhältlichen CAMICU für Intensivpatienten und dem CAM-S für Patienten auf Normalstationen. Da insbesondere das hypoaktive Delir leicht übersehen werden kann, sollte insbesondere auf Intensivstationen routinemäßig ein Screenings auf Delirien mit einem solchen standardisierten Testverfahren durchgeführt werden.
Klassifikation der Delirien
Aus klinisch-therapeutischer Sicht ist es am sinnvollsten, das Delir nach der vermuteten Ursache zu klassifizieren, also beispielsweise Delir bei Exsikkose oder Alkoholentzugsdelir.
Innerhalb dieser Gruppen kann man dann nach dem Grad der psychomotorischen Erregung in hypoaktive Delirien, Delirien vom Mischtyp und hyperaktive (agitierte) Delirien unterscheiden.
Eine weitere Differenzierung mit therapeutischer Konsequenz ist die Frage, ob es sich um ein Delir ohne psychotische Symptome/Halluzinationen oder mit psychotischen Symptomen/Halluzinationen handelt.
Man stellt sich also immer diese drei Fragen, um zu einer therapieleitenden Arbeitsdiagnose zu kommen:
- Wie ist die Psychomotorik? (Hypoaktives Delir, Delir vom Mischtyp, hyperaktives Delir)
- Welche Ursache für das Delir vermute ich? (Postoperatives Delir, Delir bei Exsikkose, Alkoholentzugsdelir, Benzodiazepinentzugsdelir, Delir, Delir bei Demenz,…)
- Liegen psychotische Symptome vor? (Delir ohne psychotische Symptome / Halluzinationen, Delir mit psychotischen Symptomen / Halluzinationen)
So entsteht eine aus diesen drei Komponenten zusammengesetzte Diagnose wie zum Beispiel „Hypoaktives postoperatives Delir ohne psychotische Symptome“ oder „Agitiertes Alkoholentzugsdelir mit psychotischen Symptomen“. Diese Art der Diagnose ist geeignet, uns den Weg zur richtigen Therapie zu leiten.
Therapie
Das Delir ist ein medizinischer Notfall, der ein zügig beginnendes und wirksames multifaktorielles Therapiekonzept erfordert.
Behandelbare Ursachen eines Delirs müssen natürlich immer zuerst behandelt werden. Zu den häufig anzutreffenden und gut behandelbaren Delirursachen gehören unter anderem Infektionen, Elektrolytstörungen, Substanzentzug, Blutzuckerentgleisungen, Schmerzen und Hypoxien. Eine ausreichende Versorgung mit Flüssigkeit gelingt oft nur durch die Gabe von Infusionen.
Wie sieht es mit der Gabe von Benzodiazepinen aus?
Früher war es üblich, jedes Delir mit Benzodiazepinen zu behandeln. Das ist inzwischen nicht mehr geboten.
Unstrittig sinnvoll ist die Gabe von Benzodiazepinen im Alkoholentzugsdelir und im Benzodiazepinentzugsdelir.
Bei allen anderen Delirien soll man Benzodiazepine oder verwandte Sedativa dann und nur dann geben, wenn eine Agitation besteht, also beim agitierten / hyperaktiven Delir oder einem Delir vom Mischtyp. Im hypoaktiven Delir soll man nach Möglichkeit keine Benzodiazepine geben. Eine Ausnahme im hypoaktiven Delir kann bestehen, wenn der Patient deutlich geängstigt wirkt, dann ist die Gabe des Benzodiazepins zur Anxiolyse sogar sinnvoll, um eine der delirverstärkenden Ursachen, die Angst, zu behandeln.
Man muss aber sagen, dass die Versorgungsrealität hier etwas anders aussieht. Es gibt viele Ärzte, die auch im hypoaktiven Delir niedrig dosiert Benzodiazepine, vorzugsweise Lorazepam, geben, in der Hoffnung, dadurch die Dauer des Delirs zu verkürzen. Dieses Vorgehen wird nicht durch Studien gestützt und es wird davon abgeraten, man sieht diese Behandlungspraxis dennoch nicht selten.
Antipsychotika
Früher war es auch üblich, bei allen Delirien Antipsychotika zu geben. Auch das ist nicht mehr indiziert.
Im Alkoholentzugsdelir und im Benzodiazepinentzugsdelir ist der Nutzen von Antipsychotika belegt1. Üblich ist die Gabe von Haloperidol, alternativ kann man auch Risperidon geben.
Bei allen anderen Delirien gilt: Man soll Antipsychotika dann und nur dann geben, wenn auch psychotische Symptome, zum Beispiel Halluzinationen bestehen.
Übersicht Therapie des Delirs

- Seitz DP, Gill SS, Psychiatry LZJOC, 2007. Antipsychotics in the treatment of delirium: a systematic review.
- Zoremba N, Coburn M. Acute confusional states in hospital. Dtsch Arztebl Int. 2019;:1–8.
- van den Boogaard M, Slooter AJC, Brüggemann RJM, et al. Effect of Haloperidol on Survival Among Critically Ill Adults With a High Risk of Delirium: The REDUCE Randomized Clinical Trial. JAMA. 2018;319(7):680–690. doi:10.1001/jama.2018.0160
- S3-Leitlinie Analgesie, Sedierung und Delirmanagement in der Intensivmedizin (DAS-Leitlinie 2015)
Copyright
Dieser Beitrag ist ein Auszug beziehungsweise eine auszugsweise Vorabveröffentlichung des Werks „Psychopharmakotherapie griffbereit“ von Dr. Jan Dreher, © Georg Thieme Verlag KG. Die ausschließlichen Nutzungsrechte liegen beim Verlag. Bitte wenden Sie sich an permissions@thieme.de, sofern Sie den Beitrag weiterverwenden möchten.
